题目内容
18.下列属于物理变化的是BA.食物腐败 B.酒精挥发C.石蜡燃烧 D.水结成冰等.
分析 本题考查学生对物理变化和化学变化的确定.判断一个变化是物理变化还是化学变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他物质的是物理变化.
解答 解:食物腐败有菌类物质生成,属于化学变化,故A错;
B、酒精挥发是由液态变为气态,只是状态发生了变化,没有新物质生成,属于物理变化,故B正确;
C、石蜡燃烧生成二氧化碳和水,属于化学变化,故C错;
D、水结冰是由液态变为固态,只是状态发生了变化,属于物理变化,
故答案为:B;水结成冰.
点评 搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变化.

练习册系列答案
相关题目
10.下列过程中发生化学变化的是( )
| A. | 铁矿石粉碎 | B. | 干冰制冷 | C. | 海水晒盐 | D. | 氢能发电 |
2.蛇纹石矿可以看做MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验流程如图1所示: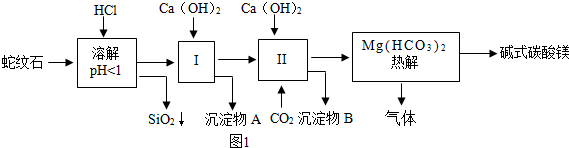
(1)蛇纹石加盐酸溶解后,溶液有Mg2+等3种金属离子产生,写出产生Mg2+的化学方程式MgO+2HCl=MgCl2+H2O.(2)进行Ⅰ操作时,控制溶液pH=6~7(有关氢氧化物沉淀的pH见表),沉淀物A中含有Fe(OH)3和Al(OH)3.该操作中Ca(OH)2不能过量,若Ca(OH)2过量,溶液pH会升高,可能导致Al(OH)3溶解,Mg(OH)2会沉淀析出.
(3)已知Mg(HCO3)2受热分解可以产生三种氧化物,请写出该反应方程式Mg(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+2CO2↑+H2O.
(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是CO2.
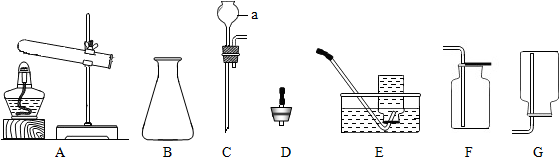
(5)确定产品碱式碳酸镁(mMgCO3•nMg(OH)2•xH2O)的组成.某同学组装仪器如图2所示:
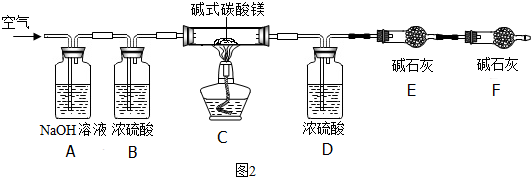
【资料查询】MgCO3、Mg(OH)2受热易分解,各生成对应的两种氧化物.
实验测得:硬质玻璃管中剩余的固体质量为2.0g,D处浓H2SO4增重0.9g,E处碱石灰增重1.76g.
①A装置中NaOH溶液的作用是除去空气中的二氧化碳;B装置中药品是除去空气中的水蒸气;在实验中要持续通入空气,其目的是使得碱式碳酸镁分解产生的二氧化碳和水蒸气被完全排出.
②通过计算可得碱式碳酸镁(mMgCO3•nMg(OH)2•xH2O)中m:n=4:1.x值为4.若将F装置去掉,对实验结果的影响是m值偏大(填“偏大”、“偏小”或“不变”).

(1)蛇纹石加盐酸溶解后,溶液有Mg2+等3种金属离子产生,写出产生Mg2+的化学方程式MgO+2HCl=MgCl2+H2O.(2)进行Ⅰ操作时,控制溶液pH=6~7(有关氢氧化物沉淀的pH见表),沉淀物A中含有Fe(OH)3和Al(OH)3.该操作中Ca(OH)2不能过量,若Ca(OH)2过量,溶液pH会升高,可能导致Al(OH)3溶解,Mg(OH)2会沉淀析出.
| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | 沉淀不溶 | 沉淀不溶 |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
| Mg(OH)2 | 8.6 | 11.1 | 沉淀不溶 | 沉淀不溶 |
(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是CO2.
(5)确定产品碱式碳酸镁(mMgCO3•nMg(OH)2•xH2O)的组成.某同学组装仪器如图2所示:

【资料查询】MgCO3、Mg(OH)2受热易分解,各生成对应的两种氧化物.
实验测得:硬质玻璃管中剩余的固体质量为2.0g,D处浓H2SO4增重0.9g,E处碱石灰增重1.76g.
①A装置中NaOH溶液的作用是除去空气中的二氧化碳;B装置中药品是除去空气中的水蒸气;在实验中要持续通入空气,其目的是使得碱式碳酸镁分解产生的二氧化碳和水蒸气被完全排出.
②通过计算可得碱式碳酸镁(mMgCO3•nMg(OH)2•xH2O)中m:n=4:1.x值为4.若将F装置去掉,对实验结果的影响是m值偏大(填“偏大”、“偏小”或“不变”).