题目内容
钙是维持人体健康正常功能所必须的元素,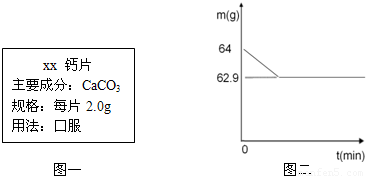
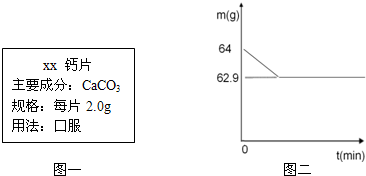
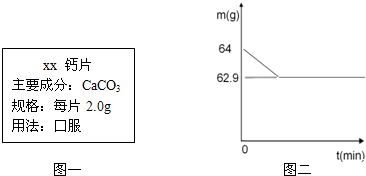
小芳服用的某种钙片说明如图一,她对钙片进行了探究:
取2片钙片,放入玻璃杯中,向其中加入60克白醋,两者恰好完全反应(假设钙片中其他成分不与白醋反应),测得玻璃杯中物质的质量与反应时间的关系如图二所示.反应的化学方程式为:CaCO3+2CH3 COOH=(CH3 COO)2Ca+H2 O+CO2↑
请你帮小芳计算:
(1)反应后产生的气体的质量为______克;
(2)两片钙片所含碳酸钙的质量;
(3)所用白醋中溶质的质量分数.
【答案】分析:(1)根据反应前后质量减少的就是二氧化碳的质量进行解答;
(2)根据二氧化碳的质量利用化学反应方程式求出碳酸钙的质量即可;
(3)根据二氧化碳的质量利用化学反应方程式求出白醋中溶质的质量进而求出所用白醋中溶质的质量分数即可;
解答:解:(1)由图可知,反应后产生的二氧化碳气体的质量为64g-62.9g=1.1g;
(2)设两片钙片所含碳酸钙的质量为x,所用白醋中溶质的质量为y.
CaCO3+2CH3COOH=(CH3COO)2Ca+H2O+CO2↑
100 120 44
x y 1.1g
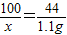
x=2.5g
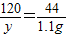
y=3g
(3)所用白醋中溶质的质量分数=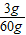 ×100%=5%
×100%=5%
答:(1)反应后产生的气体的质量为1.1g;
(2)两片钙片所含碳酸钙的质量为2.5g;
(3)所用白醋中溶质的质量分数5%.
点评:利用质量守恒定律求出反应放出二氧化碳的质量,是进行后面计算的基础,体现出运用知识分析问题的能力.
(2)根据二氧化碳的质量利用化学反应方程式求出碳酸钙的质量即可;
(3)根据二氧化碳的质量利用化学反应方程式求出白醋中溶质的质量进而求出所用白醋中溶质的质量分数即可;
解答:解:(1)由图可知,反应后产生的二氧化碳气体的质量为64g-62.9g=1.1g;
(2)设两片钙片所含碳酸钙的质量为x,所用白醋中溶质的质量为y.
CaCO3+2CH3COOH=(CH3COO)2Ca+H2O+CO2↑
100 120 44
x y 1.1g
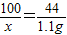
x=2.5g
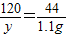
y=3g
(3)所用白醋中溶质的质量分数=
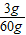 ×100%=5%
×100%=5%答:(1)反应后产生的气体的质量为1.1g;
(2)两片钙片所含碳酸钙的质量为2.5g;
(3)所用白醋中溶质的质量分数5%.
点评:利用质量守恒定律求出反应放出二氧化碳的质量,是进行后面计算的基础,体现出运用知识分析问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化学与生活密切相关。
(1)识别织物成分常用灼烧法。若灼烧时,闻到了 ,则该织物中含有羊毛。
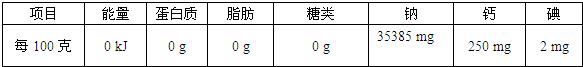
(2)“钙强化营养盐”的配料表:氯化钠、活性钙、碘酸钾。该盐中的营养成分表如下:
| 项目 | 能量 | 蛋白质 | 脂肪 | 糖类 | 钠 | 钙 | 碘 |
| 每100克 | 0 kJ | 0 g | 0 g | 0 g | 35385 mg | 250 mg | 2 mg |
①从上表中可知,此盐中含有___________种营养素。
②食用这种盐对人体健康有利的是___________(填序号)。
A.防止引起贫血病 B.维持人体内的水分和维持体液恒定的pH
C.防止甲状腺肿大 D.有助于骨骼和牙齿更坚固
③食品安全日益受到人们关注。下列食品因有毒而不能食用的是_________(填序号)。
A.甲醛浸泡的海产品 ![]() B.霉变的大米、花生
B.霉变的大米、花生
C.用亚硝酸钠(NaNO2)代替食盐烹调的食品 D.食盐腌制的咸鸭蛋
(3)正常的雨水因溶解了二氧化碳而显酸性,酸雨是指__________的雨水。
A. pH > 7 B. pH < 7 C. 5.6< pH < 7 D. pH < 5.6
(4)“节能减排”的环保理念贯穿了2010年上海世博会的全过程。下列措施不利于实现“节能减排”的是____________
A.开发使用太阳能 B.使用氢能燃料车
C.收集雨水用于绿化灌溉 D.直接将污水排入黄浦江