题目内容
15.我国化学家侯德榜发明了联合制碱法,其生产纯碱和副产品氯化铵的工艺流程如图所示: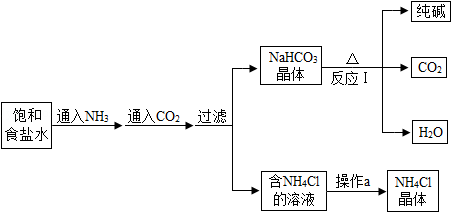
(1)NH3溶于水得到氨水,将无色酚酞溶液滴入氨水中,溶液显红色.
(2)操作a的过程是蒸发浓缩、冷却结晶、过滤.其中蒸发时用到玻璃棒的作用是防止液体受热不均而飞溅.
(3)上述工艺流程中可循环利用的物质是CO2.
分析 (1)根据碳酸钠和氨气的水溶液显碱性分析.
(2)蒸发时为防止液体溅出都要使用玻璃棒.
(3)观察分析工艺流程,找出可循环利用的物质
解答 解:(1)联合制碱法中的“碱”是纯碱,水溶液显碱性,pH大于7;NH3溶于水得到氨水,氨水显碱性,将无色酚酞溶液滴入氨水中,溶液呈红色.
(2)蒸发时,为了加快散热,防止液滴飞溅,要采用玻璃棒来搅拌,故答案为:防止液体受热不均而飞溅.
(3)由工艺流程中可知,向饱和的食盐水中通入了二氧化碳,在加热碳酸氢钠时又生成了二氧化碳,所以,可循环利用的物质是CO2.
故答案为:(1)红;
(2)防止液体受热不均而飞溅;
(3)CO2
点评 化学来源于生产、生活,又服务于生产、生活,本题很好的体现了这一理念;该题涉及化学方程式的书写,反应类型的判断等知识,要根据相关知识细心分析解答.

练习册系列答案
相关题目
14.把60g15%的某溶液分成10g,20g,30g三份,关于这三份溶液叙述中正确的是( )
①溶质质量分数相同,仍是15%;
②溶质质量相等;
③溶质质量之比1:2:3;
④性质不同、组成不同;
⑤溶质质量分数不相同,分别2.5%,5%,7.5%.
①溶质质量分数相同,仍是15%;
②溶质质量相等;
③溶质质量之比1:2:3;
④性质不同、组成不同;
⑤溶质质量分数不相同,分别2.5%,5%,7.5%.
| A. | ①③ | B. | ④⑤ | C. | ③⑤ | D. | ②③ |
20.在化学反应前后一定发生改变的是( )
①元素种类 ②原子数目 ③分子数目 ④各物质的总质量
⑤元素质量 ⑥原子种类 ⑦分子种类 ⑧物质种类.
①元素种类 ②原子数目 ③分子数目 ④各物质的总质量
⑤元素质量 ⑥原子种类 ⑦分子种类 ⑧物质种类.
| A. | ③⑤⑦ | B. | ⑦⑧ | C. | ①②⑥ | D. | ④⑧ |
7.某气体16克在氧气中充分燃烧,生成44克二氧化碳和36克水,据此可知该气体的组中一定含有的元素是( )
| A. | 碳、氢 | B. | 碳、氧 | C. | 氢、氧 | D. | 碳、氢和氧 |
4.如图为某加碘食盐包装袋上的部分文字(I为碘的元素符号).由此你得到的信息和作出的猜测是( )


| A. | 加碘食盐中的“碘”是碘单质 | |
| B. | 碘酸钾中K、I、O三元素的化合价分别为1+、5+、2- | |
| C. | 碘酸钾的相对分子质量为182 | |
| D. | 氯化钠中钠元素的质量分数约为39.3% |
5.下列关于催化剂的说法不正确的是( )
| A. | 反应前后化学性质不发生改变 | B. | 反应前后质量发生了改变 | ||
| C. | 能改变某些化学反应的速率 | D. | 某些催化剂可催化不同的反应 |
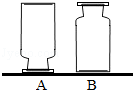 如图,在实验台上放置两瓶气体,集气瓶A、B中分别盛有二氧化碳、氧气、氢气中的一种.
如图,在实验台上放置两瓶气体,集气瓶A、B中分别盛有二氧化碳、氧气、氢气中的一种.