题目内容
14.在FeSO4和CuSO4的混合溶液中加入过量的锌粉,充分反应得到一定量固体.对固体成分的说法正确的是( )①一定含有Zn ②一定含有Fe ③一定含有Cu ④可能含有Zn ⑤可能含有Fe.
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ①②④ |
分析 在金属活动性顺序中,排在氢前面的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:在金属活动性顺序中,铜、锌、铁的活动性顺序为锌>铁>铜.所以向FeSO4和CuSO4的混合溶液中投入一些锌粉,能发生锌与硫酸铜的反应,锌与硫酸铜反应生成硫酸锌和铜,还能发生锌与硫酸亚铁的反应,锌与硫酸亚铁反应生成硫酸锌和铁,生成的铁能与硫酸铜反应生成硫酸亚铁和铜,故滤出的固体中一定有铜,③正确;向滤出的不溶物中加入少量稀硫酸,有气泡产生,则说明固体中一定含有铁,②正确,⑤错误;可能含有锌,①错误,④正确.
故选B.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
9.小红同学进行酸碱中和反应实验,反应后为确定稀盐酸和氢氧化钠溶液是否刚好完全反应,她将少量反应后的溶液,倒入一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是她得出“两种物质已恰好完全中和”的结论.
(1)写出该中和反应的化学方程式NaOH+HCl═NaCl+H2O;
(2)小霞认为小红的结论不准确,她认为除了“恰好中和”外还有一种假设,这种假设是稀盐酸过量;
(3)请你设计实验,探究小霞的假设是否成立.
(1)写出该中和反应的化学方程式NaOH+HCl═NaCl+H2O;
(2)小霞认为小红的结论不准确,她认为除了“恰好中和”外还有一种假设,这种假设是稀盐酸过量;
(3)请你设计实验,探究小霞的假设是否成立.
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入紫色石蕊试液 | 试液不变红 | 恰好中和 |
3.如图是水通电分解的示意图,从中获得的信息不正确的是( )
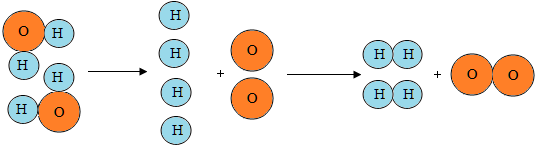
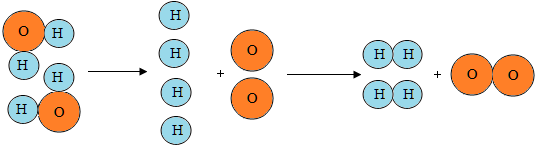
| A. | 原子是化学变化中的最小粒子 | |
| B. | 在一定条件下,水能分解生成氢气和氧气 | |
| C. | 在化学变化前后,分子和原子的种类都不变 | |
| D. | 在化学变化中,分子可以再分,原子不能再分 |
4.医用生理盐水是0.9% 的NaCl溶液,下列有关说法中,错误的是( )
| A. | 属于混合物 | B. | 溶质是氯化钠 | C. | 用前要摇匀 | D. | 静置时不分层 |
 下列物质:锌、硫酸、烧碱、乙醇、纯碱.
下列物质:锌、硫酸、烧碱、乙醇、纯碱.