题目内容
4.元素周期表是学习和研究化学的重要工具.下表是元素周期表的部分信息: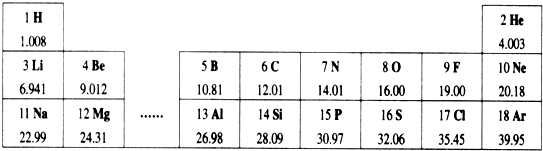
认真分析信息,回答:
(1)从表中查出硅(Si)元素的相对原子质量为28.09;
(2)已知55号元素的相对原子质量为133,则此元素的中子数为78;
(3)门捷列夫发现了元素周期律和元素周期表.
(4)研究表明,第二周期3-9号元素的原子的电子层数相同,核电荷数逐渐增大,原子核对核外电子的引力逐渐增大,故原子半径逐渐减小,试分析第三周期从11-17号元素原子半径变化规律是随核电荷数增大,原子半径逐渐减小.
(5)自己在草稿纸上画出上述三个周期的元素对应的原子结构示意图.从纵横比较可以得出许多规律,请你写出2条即可.
①同一横行元素的元素核外电子层数相同;
②同一纵行从上到下,最外层电子数相同.
分析 (1)根据从表中可查出硅元素的相对原子质量进行解答;
(2)根据原子中:核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数,结合题意进行分析解答;
(3)根据化学上常见的科学家在化学上做出的贡献,进行分析解答本题;
(4)根据元素周期表的变化规律进行解答;
(5)根据元素原子结构示意图及元素周期律知识:电子层数等于周期数;同一纵行从上到下电子层数逐渐增加;同一纵行,原子最外层电子数相同;同一周期原子的最外层电子数从左到右逐渐增加.进行解答.
解答 解:(1)从表中可查出硅元素的相对原子质量28.09;故填:28.09;
(2)因为原子中:核电荷数=核内质子数=核外电子数,由题意铯原子的核电荷数为55,故其核内质子数为55;根据相对原子质量=质子数+中子数,由题意该原子的相对原子质量为133,则中子数=133-55=78.故填:78;
(3)1869年,俄国科学家门捷列夫发现了元素周期律,并编制出元素周期表.故答案为:门捷列夫;
(4)根据元素周期表的变化规律可知:第二周期从3号--9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小.我分析第三周期从11号--17号元素原子半径变化规律是随核电荷数增大,原子半径逐渐减小;故填:随核电荷数增大,原子半径逐渐减小;
(5)根据元素原子结构示意图集元素周期律知识:电子层数等于周期数;同一纵行从上到下电子层数逐渐增加;同一纵行,原子最外层电子数相同;同一周期原子的最外层电子数从左到右逐渐增加.
故答案为:同一横行元素的元素核外电子层数相同;同一纵行从上到下,最外层电子数相同.
点评 本题考查学生对元素周期律、元素周期表知识的理解与在解题中灵活应用的能力.

练习册系列答案
相关题目
15.下列实验操作正确的是( )
| A. |  加热液体 | B. | 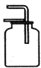 收集氧气 | C. | 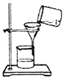 过滤 | D. | 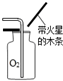 氧气验满 |
12.小靓同学为量取47mL水,第一次倒入后,仰视读数为40mL,她第二次倒入后,俯视读数为47mL,则小靓同学第二次倒入水的体积( )
| A. | 小于7mL | B. | 大于7mL | C. | 等于7mL | D. | 无法确定 |
19.“达菲”是治疗甲型“H1N1流感”的一种特效药.该药物的主要成分是一种化学式为C16H31N2PO8的物质.下列叙述中错误的是( )
| A. | C16H31N2PO8的相对分子质量为410 | |
| B. | C16H31N2PO8中氢元素和磷元素的质量分数相同 | |
| C. | “达菲”是纯净物 | |
| D. | C16H31N2PO8由五种元素组成 |
14.知道一些家庭防火知识和紧急灭火措施,就能避免火灾,下列说法你认为不正确的是( )
| A. | 及时更换老化破损电线,修理失灵电器 | |
| B. | 电器着火应用水扑灭 | |
| C. | 油锅中的油着火,可用锅盖盖灭 | |
| D. | 室内起火时不要急于打开门窗 |
 海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,它们的溶解度曲线如图甲所示,试完成下列各题:
海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,它们的溶解度曲线如图甲所示,试完成下列各题: