题目内容
增白剂的主要成分是过氧化苯甲酰,化学式为C14H10O4,下列说法正确的是( )
| A、C14H10O4由C、H、O元素组成 |
| B、C14H10O4的相对分子质量为242g |
| C、C14H10O4中O元素的质量分数最高 |
| D、60.5g C14H10O4和22g CO2中所含O元素质量相等 |
考点:化学式的书写及意义,相对分子质量的概念及其计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学用语和质量守恒定律
分析:根据过氧化苯甲酰的化学式为C14H10O4,分析其构成和组成,再利用相对原子质量来 计算元素的质量分数.
解答:解:A、由过氧化苯甲酰的化学式为C14H10O4,该物质是由C、H、O三种元素组成,故A正确;
B、据对分子质量的计算方法,C14H10O4的相对分子质量为:12×14+1×10+16×4=242’而非242g,故B错误;
C、由过氧化苯甲酰的化学式为C14H10O4,氧元素的质量分数为X=
×100%,碳元素的质量分数为y=
×100%,y大于X,故C错误;
D、60.5g C14H10O4中所含O元素质量为:60.5g×
×100%=16g
22g CO2中所含O元素质量为22g×
×100%=16g
故D正确.
故选:A、D.
B、据对分子质量的计算方法,C14H10O4的相对分子质量为:12×14+1×10+16×4=242’而非242g,故B错误;
C、由过氧化苯甲酰的化学式为C14H10O4,氧元素的质量分数为X=
| 16×4 |
| 12×14+1×10+16×4 |
| 12×14 |
| 12×14+1×10+16×14 |
D、60.5g C14H10O4中所含O元素质量为:60.5g×
| 16×4 |
| 12×14+1×10+16×4 |
22g CO2中所含O元素质量为22g×
| 16×2 |
| 12+16×2 |
故D正确.
故选:A、D.
点评:本题以生活中的食品添加剂为信息来考查学生利用物质的化学式来分析解答问题,明确其组成和构成在语言描述上的差别及正确使用信息来解答本题即可.

练习册系列答案
相关题目
分子与原子的本质区别在于( )
| A、分子是构成物质的一种粒子 |
| B、分子在不停地运动着 |
| C、分子之间有空隙 |
| D、在化学变化中,分子可分,原子不可分 |
生活中的下列做法或说法正确的是( )
| A、用工业用盐(亚硝酸钠)腌制火腿 |
| B、多食海带可防治缺铁性贫血 |
| C、食用含钙食品可预防佝偻病 |
| D、霉变的大米洗净后可以放心食用 |
水在灭火中的主要作用( )
| A、降低可燃物的着火点 |
| B、使大火隔绝空气 |
| C、降低温度 |
| D、水分解出不能助燃的气体 |
除去下列各混合物中的杂质[括号内的物质为杂质],所采用的方法正确的是( )
| A、除去CO2中的[CO]杂质; 采用的方法:在空气中燃烧 |
| B、除去KCl中的[KClO3]杂质; 采用的方法:加入二氧化锰后受热分解 |
| C、除去CO2中的[O2]杂质; 采用的方法:通过炽热炭层 |
| D、除去Cu粉中的[CuO]杂质; 采用的方法:在加热条件下用CO还原 |
M、X、Y、Z四种物质在一定条件下,存在如下转化关系:①M+X→Y②Y+Z→X+N③M+Z→X+N其中X是一种无色无味且能使澄清石灰水变浑浊的气体,N是一种光亮红色的金属.下列判断中,正确的是( )
| A、Z一定是CuO |
| B、M一定是CO |
| C、Y可能是H2 |
| D、M可能是C或CO |
元素、原子、分子等概念之间有联系和区别,下列描述正确的是( )
| A、物质是由元素构成 |
| B、化学变化中分子、原子种类都保持不变 |
| C、分子可以再分,原子不可以再分 |
| D、分子可以构成物质,原子也能构成物质 |
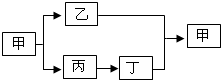 甲乙丙丁是初中化学常见的化合物,甲和乙中含有碳元素,丙能做干燥剂.它们之间有如图所示的转化关系(部分物质和反应条件已略去).
甲乙丙丁是初中化学常见的化合物,甲和乙中含有碳元素,丙能做干燥剂.它们之间有如图所示的转化关系(部分物质和反应条件已略去).