题目内容
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的 Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )
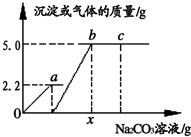
| A.图中0a段表示生成沉淀的过程 |
| B.b点溶液中溶质有2种 |
| C.c点溶液的pH=7 |
| D.x值为106.0 |

A、图中oa段表示生成的气体质量,故A选项错误;
B、b点表示碳酸钠恰好完全反应,溶液中只含有NaCl一种溶质,故B选项错误;
C、c点的溶液中含有Na2CO3、NaCl两种溶质,由于Na2CO3显碱性,NaCl显中性,所以c的溶液的pH>7;故C选项错误;
D、根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知碳酸钠与盐酸反应生成气体2.2g,碳酸钠与氯化钙反应,生成沉淀5.0g.设生成2.2g气体所需的Na2CO3的质量为y,生成沉淀5.0g所需Na2CO3的质量为z.则
Na2CO3~CO2↑
106 44
y 2.2
=
解得y=5.3g;
Na2CO3~CaCO3↓
106 100
z 5.0g
=
解得z=5.3g;
所以x=
=106.0g;
故D选项正确;
故选D.
B、b点表示碳酸钠恰好完全反应,溶液中只含有NaCl一种溶质,故B选项错误;
C、c点的溶液中含有Na2CO3、NaCl两种溶质,由于Na2CO3显碱性,NaCl显中性,所以c的溶液的pH>7;故C选项错误;
D、根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知碳酸钠与盐酸反应生成气体2.2g,碳酸钠与氯化钙反应,生成沉淀5.0g.设生成2.2g气体所需的Na2CO3的质量为y,生成沉淀5.0g所需Na2CO3的质量为z.则
Na2CO3~CO2↑
106 44
y 2.2
| 106 |
| y |
| 44 |
| 2.2 |
解得y=5.3g;
Na2CO3~CaCO3↓
106 100
z 5.0g
| 106 |
| z |
| 100 |
| 5.0g |
解得z=5.3g;
所以x=
| 5.3g+5.3g |
| 10% |
故D选项正确;
故选D.

练习册系列答案
相关题目
 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的 Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的 Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )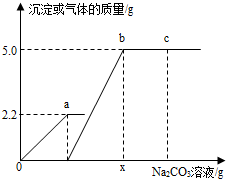

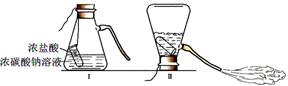
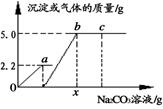
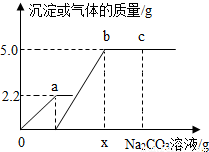 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的 Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的 Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )