题目内容
1. 黄铜是铜与锌的合金,因色黄而得名.黄铜的机械性能和耐磨性能都很好,可用于制造精密仪器、船舶的零件、枪炮的弹壳等.
黄铜是铜与锌的合金,因色黄而得名.黄铜的机械性能和耐磨性能都很好,可用于制造精密仪器、船舶的零件、枪炮的弹壳等.(1)在常见物质分类中,黄铜属于合金.
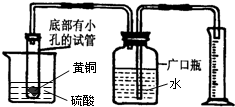
(2)小刚同学想对一块黄铜中所含锌、铜的质量分数进行 粗略测定,设计了如图所示的实验装置.实验的基本思路:利用合金与酸反应产生的气体,通过如图实验装置把水排到量筒中,读出量筒中水的体积(不考虑其它因素的影响,反应产生的气体体积即为量筒中水的体积),可计算锌铜合金中锌、铜的质量分数.
小刚同学在实验过程中选取了3g锌铜合金与足量的稀硫酸,反应完全后,量筒中接收的液体的体积为0.2升,求锌、铜合金中锌的质量分数是多少?(氢气的密度为0.09克/升)
(反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑)
(3)现取一块部分被氧化成氧化镁的镁条,能否用上述方法测出该镁条中单质镁的质量分数,并说明理由:能;锌与酸反应产生气体,而氧化锌与酸反应不产生气体.
分析 (1)根据黄铜属于合金解答;
(2)通过测定合金与酸反应产生氢气的体积来测定合金锌、铜的质量分数;
(3)此合金中是锌与稀硫酸反应产生氢气,要根据氢气的质量,利用化学方程式求锌的质量.
解答 解:
(1)黄铜属于合金;
(2)根据“量筒中接收的液体的体积为0.2L”,氢气的体积为0.2L,因为氢气的密度为0.09g/L,故其质量为0.09g/L×0.2L=0.018g;
设生成0.0089g氢气,需要锌的质量为x.
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.018g
$\frac{65}{x}=\frac{2}{0.018g}$
x=0.585g
故锌、铜合金中锌的质量分数是$\frac{0.585g}{3g}×$100%=19.5%
(3)如要测定部分被氧化成氧化锌的锌粒中锌单质的质量分数,能用上述实验方法.因为锌与酸反应产生气体,而氧化锌与酸反应不产生气体.
故答案为:
(1)合金;
(2)19.5%;
(3)能;锌与酸反应产生气体,而氧化锌与酸反应不产生气体.
点评 本题考查了金属性质的应用,要测定其中某成分的含量,可以使其发生化学反应,而另一种金属不反应.根据生成物质的质量来进行起算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列化学方程式正确的是( )
| A. | BaCl2+Mg(NO3)2═Ba(NO3)2↓+MgCl2 | B. | Na2SO4+BaCO3═BaSO4↓+Na2CO3 | ||
| C. | Mg+2AgCl═MgCl2+2Ag | D. | 2Al+3CuCl2═2AlCl3+3Cu |
16. 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )
 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )| A. | x值为53.0 | B. | c点溶液的pH=7 | ||
| C. | b点溶液中溶质只有1种 | D. | 图中Oa段表示生成沉淀的过程 |
 目前,市场上出现的木糖醇(化学式为C5H12O5)是一种新型甜味剂.试回答下列问题:
目前,市场上出现的木糖醇(化学式为C5H12O5)是一种新型甜味剂.试回答下列问题: 在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是里面含有氯化铁的缘故.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小明做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系.
在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是里面含有氯化铁的缘故.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小明做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系.
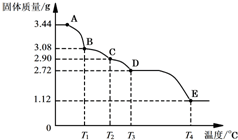 CaSO4•2H2O受热会逐步失去结晶水.取纯净的CaSO4•2H2O固体3.44g进行加热,测定固体质量随温度的变化情况如图所示.C点固体的化学式是2CaSO4•H2O.T3~T4温度段加热固体所产生的气体是形成酸雨的主要物质之一,则D~E段发生反应的化学方程式为2CaSO4$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+O2↑.
CaSO4•2H2O受热会逐步失去结晶水.取纯净的CaSO4•2H2O固体3.44g进行加热,测定固体质量随温度的变化情况如图所示.C点固体的化学式是2CaSO4•H2O.T3~T4温度段加热固体所产生的气体是形成酸雨的主要物质之一,则D~E段发生反应的化学方程式为2CaSO4$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+O2↑.