题目内容
16.在实验室中,某同学发现了一瓶敞口放置的氢氧化钙粉末试剂,并对其产生兴趣,进行如下实验.
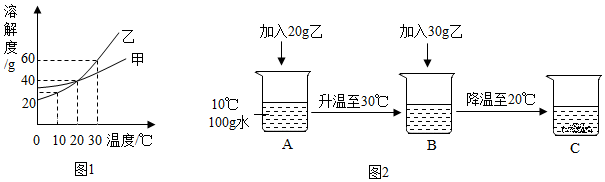
根据实验过程和图象提供的信息,回答下列问题:
(1)完全反应后生成气体的质量是2.2g.
(2)b点溶液中的溶质为氯化钙和氯化氢(填名称).
(3)求恰好完全反应时所得溶液中溶质的质量分数?(利用化学方程式进行计算,书写计算过程,结果精确到0.1%)
分析 (1)根据和碳酸钙反应的盐酸为25g且质量分数为14.6%计算生成的二氧化碳的质量;
(2)b点是盐酸过量的,所以溶质为剩余的氯化氢和生成的氯化钙;
(3)由于氯元素守恒,根据关系式法求算氯化钙的质量,进而求算其质量分数.
解答 解:
(1)由于和碳酸钙反应的盐酸为25g且质量分数为14.6%,所以对应溶质的质量为25g×14.6%=3.65g
设生成的二氧化碳的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
3.65g x
$\frac{73}{44}$=$\frac{3.65g}{x}$
x=2.2g
(2)b点是盐酸过量的,所以溶质为剩余的氯化氢和生成的氯化钙
(3)设生成的氯化钙的质量为y.
由于氯元素守恒,所以可得关系式2HCl∽∽∽CaCl2
2HCl∽∽∽∽∽∽∽∽CaCl2
73 111
75g×14.6% y
$\frac{73}{111}$=$\frac{75g×14.6%}{y}$
y=16.65g
恰好完全反应时所得溶液中溶质的质量分数为$\frac{16.65g}{12.4g+80.0g+75g-2.2g}$×100%≈10.1%
答:(1)完全反应后生成气体的质量是 2.2g.
(2)b点溶液中的溶质为 氯化钙和氯化氢.
(3)恰好完全反应时所得溶液中溶质的质量分数为10.1%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
6.互为同素异形体的一组物质是( )
| A. | 金刚石和石墨 | B. | 铁粉和铁丝 | C. | 液氧和氧气 | D. | 银和汞 |
7.将一定质量的Zn加入到Mg(NO3)2、Fe(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,滤液仍为浅绿色,则下列判断正确的是( )
| A. | 滤渣一定为Ag、Fe | |
| B. | 向滤液中滴加稀盐酸,可能产生白色沉淀 | |
| C. | 滤液中最多含有三种溶质 | |
| D. | 反应前后金属固体的质量可能不变 |
4.分析和推理是学习和研究化学的重要方法.下列说法正确的是( )
| A. | 有机物一定含有碳元素,则含碳元素的化合物也一定是有机物 | |
| B. | 同种元素的原子质子数相同,则质子数相同的原子一定是同种元素 | |
| C. | 氧化物一定含有氧元素,则含有氧元素的化合物一定是氧化物 | |
| D. | 中和反应生成盐和水,则生成盐和水的反应一定是中和反应 |
1.下列实验操作不正确的是( )
| A. | 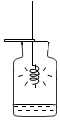 铁丝燃烧 | B. | 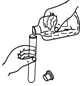 倾倒液体 | C. | 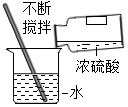 稀释浓硫酸 | D. |  仪器连接 |
8.英国化学家亨利•卡文迪许是燃素说的信仰者.1766年,他用铁、锌、锡等六种金属与稀硫酸、稀盐酸作用制得“可燃空气”.并将其表示为:
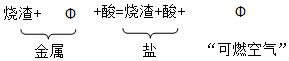
用所学化学知识判断.下列说法正确的是( )

用所学化学知识判断.下列说法正确的是( )
| A. | “可燃空气”是从金属中分解出来的 | B. | 上述六种金属包括铜 | ||
| C. | “可燃空气”可以用排水集气法收集 | D. | 上述反应属于复分解反应 |
5.下列实验现象的描述,正确的是( )
| A. | 硫在空气中燃烧,产生明亮的蓝紫色火焰 | |
| B. | 打开浓盐酸的试剂瓶,瓶口会出现白雾 | |
| C. | 一氧化碳还原氧化铁,固体由黑色变红色 | |
| D. | 把铁钉放入硫酸铜溶液中,有铜析出 |
11.“五月端午粽飘香”,粽子的主要食材是糯米,其富含的营养素是( )
| A. | 糖类 | B. | 油脂 | C. | 蛋白质 | D. | 维生素 |