题目内容
甲、乙两工厂排出的废水澄清透明,分别含有K+Ba2+Cu2+OH-CO32-NO3-六种离子中的三种不同的离子,已知甲厂废水明显呈碱性.若两厂单独排放都会造成严重的污染;若将两厂的污水按一定比例混合,沉淀后污水会变成只含一种溶质的无色澄清溶液,此溶质可做化肥.下列关于污水的分析中,正确的是
A.甲厂排放的废水中含有K+、Ba2+、OH一三种离子
B.甲厂排放的废水中含有K+、OH一、CO32一三种离子
C.可做化肥的溶质为KNO3
D.可做化肥的溶质为K2CO3
答案:BC
解析:
解析:
|
本题考查复分解反应及离子不共存知识.因甲厂废水明显呈碱性,所以甲中废水必含OH一,则与OH一不能共存的离子Cu2+一定在乙废水中,与Cu2+不能共存的CO32-一定在甲废水中,与CO32-不能共存的Ba2+一定在乙废水中,再根据溶液呈电中性,所以NO3-一定在乙中,K+一定在甲中,甲乙废水混合后生成的可溶性物质是KNO3属于一种复合肥料. |

练习册系列答案
相关题目
 --氧原子、
--氧原子、 --氮原子、
--氮原子、 --碳原子):
--碳原子):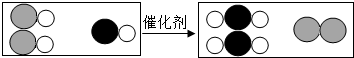
 --氧原子、
--氧原子、 --氮原子、
--氮原子、 --碳原子):
--碳原子):
 --氧原子、
--氧原子、 --氮原子、
--氮原子、 --碳原子):
--碳原子):