题目内容
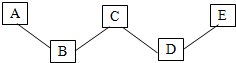
8. 氧化还原反应是指反应前后元素的化合价发生变化的反应.如图概括了四种基本反应类型与氧化还原反应的关系,下列反应所在图示位置的说法错误的是( )
氧化还原反应是指反应前后元素的化合价发生变化的反应.如图概括了四种基本反应类型与氧化还原反应的关系,下列反应所在图示位置的说法错误的是( )| A. | Ca(OH)2+Na2CO3═CaCO3↓+2NaOH可放在①位置 | |
| B. | 实验室制取氢气的反应以及铁和硫酸铜溶液的反应可放在③位置 | |
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑和水分解的反应可放在②位置 | |
| D. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2是氧化还原反应可放在③位置 |
分析 根据题意,氧化还原反应是指反应前后元素的化合价发生变化的反应,据此结合四种基本反应类型的特征,进行分析判断.
解答 解:A、复分解反应是两种化合物相互交换成分生成两种新的化合物的反应,特征是换成分,价不变,一定不属于氧化还原反应,故可放在①的位置;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,该反应属于复分解反应,可放在①的位置,故选项说法正确.
B、③全部属于氧化还原反应,置换反应反应前后一定有元素的化合价发生变化,一定属于氧化还原反应,故③是置换反应;实验室制取氢气,采用的是锌与稀硫酸反应生成硫酸锌和氢气,属于置换反应,可放在③位置,故选项说法正确.
C、②位置的反应是分解反应,CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑、水分解的反应均属于分解反应,可放在②位置,故选项说法正确.
D、由B选项的分析,③是置换反应;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,但该反应的反应物均为化合物,不属于置换反应,故不能放在③位置,故选项说法错误.
故选:D.
点评 本题难度不大,充分理解氧化还原反应的含义、四种基本的反应类型的特征是正确解题的关键.

练习册系列答案
相关题目
19.甲同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬的.她想到在学过的金属活动性顺序中并没有金属铬,为比较铬与常见金属铁、铜的活动性强弱,她和同学们在应用所学知识进行分析的基础上,提出了以下猜想,并进行了实验探究.
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
①铬(Cr)是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【实验药品】
铁片、铬片、铜片、稀硫酸、CuSO4溶液、CrSO4溶液、FeSO4溶液.(溶液均为新制)
【甲同学实验】
甲同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的稀硫酸.
【乙同学实验】
乙同学为验证甲同学的结论,又设计了以下实验.
【实验反思】
(1)你认为乙同学没有必要做的实验是试管5中的实验没有必要做.
(2)请你结合所给的实验药品再设计一个实验,验证甲同学的结论.
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
①铬(Cr)是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【实验药品】
铁片、铬片、铜片、稀硫酸、CuSO4溶液、CrSO4溶液、FeSO4溶液.(溶液均为新制)
【甲同学实验】
甲同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的稀硫酸.
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管1 | 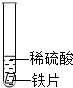 | 铁片表面产生气泡较慢,溶液变为浅绿色. | (1)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜的. (2)甲同学得到的结论是猜想1正确. |
| 试管2 |  | 铬片表面产生气泡较快,溶液变为蓝色. | |
| 试管3 | 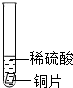 | 铜片上没有变化 |
乙同学为验证甲同学的结论,又设计了以下实验.
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管4 | 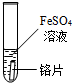 | (1)甲同学的结论正确. (2)请写出铬与硫酸铜反应的化学方程式Cr+CuSO4=CrSO4+Cu. | |
| 试管5 |  |
(1)你认为乙同学没有必要做的实验是试管5中的实验没有必要做.
(2)请你结合所给的实验药品再设计一个实验,验证甲同学的结论.
| 实验操作和实验现象 | 结论与解释 |
| 甲同学的结论正确. |
20.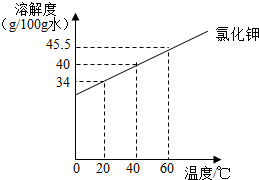 根据下表实验,回答相关问题.
根据下表实验,回答相关问题.
(1)实验步骤Ⅱ中加入Xg氯化钾,X=9g.
(2)实验步骤Ⅳ中所得溶液是饱和(填“饱和”或“不饱和”)溶液.
(3)步骤Ⅴ中冷却至20℃,烧杯中的现象是有晶体析出.
(4)有五瓶氯化钾溶液,与上述实验步骤Ⅰ-Ⅴ形成的溶液溶质质量分数分别相等,现各取10g于5个小烧杯中,分别滴入足量的等质量等质量分数的硝酸银溶液,其中有3个小烧杯中产生的沉淀质量相等.
 根据下表实验,回答相关问题.
根据下表实验,回答相关问题.| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 在盛有100g水的烧杯中,加入25g氯化钾,搅拌,恢复到20℃ | 全部溶解 |
| Ⅱ | 再加Xg氯化钾,搅拌,恢复到20℃,恰好饱和 | 全部溶解 |
| Ⅲ | 再加6g氯化钾,搅拌,恢复到20℃ | 固体不溶 |
| Ⅳ | 加热至40℃ | 全部溶解 |
| Ⅴ | 冷却至20℃ |
(2)实验步骤Ⅳ中所得溶液是饱和(填“饱和”或“不饱和”)溶液.
(3)步骤Ⅴ中冷却至20℃,烧杯中的现象是有晶体析出.
(4)有五瓶氯化钾溶液,与上述实验步骤Ⅰ-Ⅴ形成的溶液溶质质量分数分别相等,现各取10g于5个小烧杯中,分别滴入足量的等质量等质量分数的硝酸银溶液,其中有3个小烧杯中产生的沉淀质量相等.
17.某物质在氧气中充分燃烧只生成二氧化碳,关于该物质的组成说法错误的是( )
| A. | 该物质可能是C60 | B. | 该物质一定是碳单质 | ||
| C. | 该物质一定不是甲烷 | D. | 该物质中一定含有碳元素 |
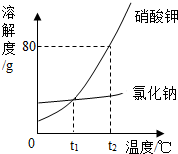 如图是氯化钠与硝酸钾的溶解度曲线,回答:
如图是氯化钠与硝酸钾的溶解度曲线,回答: