题目内容
18.小浩是班上的小小化学家,最近对蜡烛产生了兴趣,于是开始了系列实验.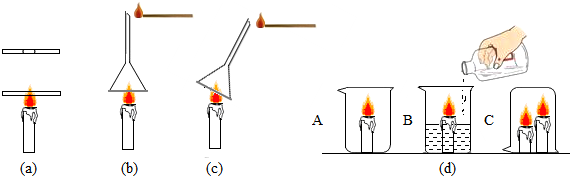
(1)如图(a),将一根火柴棒置于火焰上,火柴棒的变化如图所示,说明火焰的外焰处温度最高.
(2)如图(b),在火焰正上方罩一个普通漏斗,用一燃着的火柴接近漏斗颈口处,可观察到火焰熄灭了,原因是蜡烛燃烧产生热的二氧化碳气体上升,二氧化碳不支持燃烧.
(3)如图(c),将漏斗斜插入蜡烛焰心时,观察到漏斗内产生白烟,漏斗颈口处被点燃,产生了黄色火焰,你判断白烟的主要成分是汽化的石蜡蒸汽.
(4)如图(d),他在B烧杯中先加入适量的碳酸钠粉末,分别点燃四支蜡烛,然后在B杯中加入稀盐酸,将C烧杯倒罩在高矮不同的两支蜡烛上.在A、B两烧杯中,蜡烛先熄灭的是B,C烧杯中先熄灭的是较高(填“高”或“矮”)的蜡烛,理由是烧杯容积较小,燃烧产生热的二氧化碳气体上升后自上而下覆盖在烧杯中,由此我们可以得到启发:从着火燃烧的高楼房间中逃离,正确的方法是AC.
A.用毛巾捂住口鼻 B.成站立姿势跑出 C.沿墙角迅速爬向门外 D.打开窗户跳出
(5)为了探究蜡烛的组成,他取了个干冷的小烧杯罩在火焰上方,发现杯壁有水雾出现,将小烧杯迅速倒置,倒入澄清石灰水,振荡,发现石灰水变浑浊,据此他得出关于蜡烛组成的结论是蜡烛中一定含有碳元素、氢元素,还可能含有氧元素.
分析 (1)根据蜡烛燃烧现象及是否生成新物质解答;
(2)根据火焰的分层情况分析;
(3)根据蜡烛燃烧生成物分析解答;
(4)根据碳酸钠与稀盐酸反应能快速产生大量二氧化碳气体及二氧化碳的性质解答;
(5)根据蜡烛燃烧生成物结合质量守恒定律分析解答.
解答 解:
(1)蜡烛火焰是分层的,中间无变化,两边烧焦,说明外焰温度最高,焰心温度最低;
(2)蜡烛燃烧生成二氧化碳和水,因此,在火焰正上方罩一个普通漏斗,用一燃着的火柴接近漏斗颈口处,可观察到火焰熄灭,
(3)插入蜡烛焰心时,汽化的石蜡蒸汽会被导出,其具备可燃性,故燃烧;
(4)蜡烛燃烧产生的少量二氧化碳及时B散失到空气中,碳酸钠与盐酸反应快速产生大量二氧化碳,二氧化碳不能燃烧,也不支持燃烧,故B中蜡烛先熄灭;C杯中先熄灭的是较高的蜡烛,因为烧杯容积小,燃烧产生热的二氧化碳上升后自上而下覆盖在烧杯中,故高的先灭;
用毛巾捂住鼻子可以防止吸入一些烟尘等有害物质;由以上实验获知燃烧时产生的二氧化碳等气体会上升,故因采取较低的姿势逃生.在高楼打开窗户跳出生存的机会不是很大.
(5)蜡烛燃烧生成水和二氧化碳,故干冷的杯壁有水雾生成,澄清的石灰水变浑浊,根据质量守恒定律反应前后元素的种类不变,故蜡烛中肯定含有碳元素、氢元素,但不一定含氧元素,因为反应物中有氧气参加,提供了氧元素;
答案:
(1)外焰;
(2)蜡烛燃烧产生热的二氧化碳气体上升,二氧化碳不支持燃烧;
(3)汽化的石蜡蒸汽;
(4)B;高;烧杯容积较小,燃烧产生热的二氧化碳气体上升后自上而下覆盖在烧杯中;AC;
(5)变浑浊;碳元素、氢;
点评 本题对蜡烛燃烧的现象,生成物、二氧化碳的性质、质量守恒定律的应用等知识进行了考查,通过做题告诉学生实验时要认真观察、分析.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.用锌、氧化铜、稀硫酸作原料,采取下列两条途径制取铜:
①Zn $\stackrel{稀硫酸}{→}$H2 $\stackrel{CuO}{→}$Cu
②CuO $\stackrel{稀硫酸}{→}$CuSO4 $\stackrel{Zn}{→}$Cu
若这两种方法制得的铜的质量相等,则下列叙述符合实际实验结果的是( )
①Zn $\stackrel{稀硫酸}{→}$H2 $\stackrel{CuO}{→}$Cu
②CuO $\stackrel{稀硫酸}{→}$CuSO4 $\stackrel{Zn}{→}$Cu
若这两种方法制得的铜的质量相等,则下列叙述符合实际实验结果的是( )
| A. | 一定消耗相同质量的氧化铜 | B. | 一定消耗相同质量的锌 | ||
| C. | 消耗的稀硫酸的质量不相同 | D. | 一定生成相同质量的硫酸锌 |
10.下列物质中属于纯净物的是( )
| A. | 空气 | B. | 海水 | C. | 冰和水混合 | D. | 澄清的石灰水 |