题目内容
2011年,日本福岛第一核电站发生核辐射泄漏,产生放射性碘-131,可能被附近居民吸入,引发甲状腺疾病或甲状腺癌.请回答下列问题:
(1)世界卫生组织提示要求谨慎服用碘片,以减少人体甲状腺吸收放射性碘.碘片的主要成分为碘化钾(化学式为KI),则碘化钾中碘元素化合价为 .推荐服用量为每天100毫克碘元素(碘、钾的相对原子质量分别为127、39),某品牌碘片剂每颗含有10毫克碘化钾,则每天需要服用 颗碘片剂.
(2)每500g加碘食盐,经化验其中含有碘元素 50mg,我们每天食用10g碘盐,则我们从碘盐中可吸收 mg碘元素,食用碘盐 (能否)防治核辐射.
(1)世界卫生组织提示要求谨慎服用碘片,以减少人体甲状腺吸收放射性碘.碘片的主要成分为碘化钾(化学式为KI),则碘化钾中碘元素化合价为
(2)每500g加碘食盐,经化验其中含有碘元素 50mg,我们每天食用10g碘盐,则我们从碘盐中可吸收
考点:有关元素化合价的计算,化合物中某元素的质量计算
专题:化学与生活
分析:(1)根据在化合物中正负化合价代数和为零求出化合价;用100毫克碘元素除以每颗碘片剂中碘元素的质量就是服用的颗数;
(2)根据题意,每500g加碘食盐,经化验其中含有碘元素50mg,据此可以计算出10g碘盐中碘元素的质量.每人日服用含碘100mg的碘片才能有效阻止放射性碘的辐射,根据每天10g食用碘盐的碘元素质量,可以判断食用碘盐能否防止核辐射.
(2)根据题意,每500g加碘食盐,经化验其中含有碘元素50mg,据此可以计算出10g碘盐中碘元素的质量.每人日服用含碘100mg的碘片才能有效阻止放射性碘的辐射,根据每天10g食用碘盐的碘元素质量,可以判断食用碘盐能否防止核辐射.
解答:解:(1)在化学式KI中,K为+1价,根据化合价代数和为零的原则,可知I的化合价为-1价;需要服用碘片剂的颗数为100 mg÷(10 mg×
)≈13;
(2)每天食用10g碘盐,从中吸收的碘元素质量为:
×50mg=1 mg,由此可知食用碘盐不能防治核辐射.
故答案为:(1)-1;13;(2)1;不能.
| 127 |
| 127+39 |
(2)每天食用10g碘盐,从中吸收的碘元素质量为:
| 10g |
| 500g |
故答案为:(1)-1;13;(2)1;不能.
点评:学来源于生产生活,也必须服务于生产生活,与人类生产生活相关的化学知识也是重要的中考热点之一;本题以碘盐为素材,考查了学生运用化学知识分析解决实际问题的能力.

练习册系列答案
相关题目
反应中,若反应物中某种元素化合价升高就是氧化反应,则下列是发生氧化反应的是( )
| A、O2→H2O |
| B、KMnO4→K2MnO4 |
| C、H2SO4→H2 |
| D、NO2→NO3- |

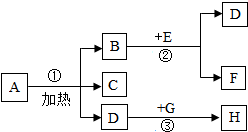 在如图转化关系中,生成物D能使带火星的木条复燃,H能使澄清石灰水变浑浊,在反应②中,B的质量和化学性质均没有改变.
在如图转化关系中,生成物D能使带火星的木条复燃,H能使澄清石灰水变浑浊,在反应②中,B的质量和化学性质均没有改变.
 某化肥包装袋上的部分说明如右图所示.
某化肥包装袋上的部分说明如右图所示. ,该化学式表示由n个CF2=CF2分子聚合在一起组成一个大分子,该有机高分子材料中所含碳、氟元素的质量比为
,该化学式表示由n个CF2=CF2分子聚合在一起组成一个大分子,该有机高分子材料中所含碳、氟元素的质量比为