题目内容
12. 某校九年级(3)班的几个同学利用鸡蛋壳制取二氧化碳,并对二氧化碳的性质进行验证,实验装置如图所示(鸡蛋壳的主要成分是碳酸钙):
某校九年级(3)班的几个同学利用鸡蛋壳制取二氧化碳,并对二氧化碳的性质进行验证,实验装置如图所示(鸡蛋壳的主要成分是碳酸钙):当打开K,反应一段时间后:
(1)B处可以观察到的现象是紫色石蕊溶液变成红色.
(2)C处澄清石灰水变浑浊,写出反应的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O.
(3)D处烧杯中下层(选填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的物理性质是密度比空气的大.
(4)A中用于添加液体的仪器名称:长颈漏斗,写出A处制取二氧化碳的化学方程式:2HCl+CaCO3═CaCl2+H2O+CO2↑.
(5)若用A装置来做实验室制取氧气的发生装置,则该装置中发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 (1)根据显酸性的溶液能使石蕊试液变红色进分析;
(2)根据二氧化碳能使澄清石灰水变浑浊进行分析;
(3)根据实验现象可以判断二氧化碳的物理性质和化学性质;
(4)根据鸡蛋壳的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳进行分析;
(5)根据装置特点来确定制取方法.
解答 解:(1)二氧化碳能和水反应生成碳酸,碳酸能使紫色石蕊溶液变红,故B处紫色石蕊溶液变成红色;故填:紫色石蕊溶液变成红色;
(2)二氧化碳能和氢氧化钙溶液反应生成碳酸钙沉淀和水,该反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;故填:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)二氧化碳不燃烧也不支持燃烧以及二氧化碳的密度大于空气的密度,所以D烧杯中下层的蜡烛先熄灭.故填:下层;密度比空气的大;
(4)A是长颈漏斗;鸡蛋壳中的碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.故填:长颈漏斗;2HCl+CaCO3═CaCl2+H2O+CO2↑;
(5)装置制取氧气的反应物是固体和液体,反应条件是常温,所以反应物是过氧化氢,过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 本题是课本知识内容的再现,主要训练有关二氧化碳性质的熟练掌握程度,考查内容简单注重基础.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
7.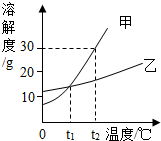 甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中错误的是( )
甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中错误的是( )
 甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中错误的是( )
甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中错误的是( )| A. | t1℃时,甲物质的溶解度与乙物质的溶解度相等 | |
| B. | t2℃时,将50 g甲物质放入100 g水中,所得溶液的质量为150 g | |
| C. | 升高温度可将乙物质的饱和溶液变为不饱和溶液 | |
| D. | 当甲物质中含少量乙物质时,可用蒸发结晶的方法提纯甲物质 |
17.中国中医研究院终身研究员兼首席研究员屠呦呦创制了新型抗疟药--青蒿素(C15H22O5)和双氢青蒿素(C15H24O5)获得获得2015年诺贝尔医学奖,关于青蒿素说法中正确的是( )
| A. | 青蒿素属于有机物 | |
| B. | 青蒿素中碳、氢、氧三种元素的质量比是15:22:5 | |
| C. | 青蒿素由15个原子、22个氢原子和5个氧原子构成 | |
| D. | 青蒿素和双氢青蒿素化学性质完全相同 |
1.除去下列物质中少量杂质所加入试剂合理的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质所加试剂 |
| A | Ca(OH)2 | CaCO3 | 盐酸 |
| B | MgCl2 | NaCl | 硝酸银溶液 |
| C | C | Fe | 稀硫酸 |
| D | CO2 | HCl | 氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
16.填写下列除杂所用的试剂或主要操作(操作选填序号):
除杂操作:a.过滤 b.蒸发 c.洗气 d.高温煅烧 e.加热
除杂操作:a.过滤 b.蒸发 c.洗气 d.高温煅烧 e.加热
| 组别 | 物质 | 杂质 | 除杂所用的试剂 | 除杂操作 |
| ① | Cu | CuO | 稀硫酸 | a |
| ② | HCl溶液 | H2SO4 | 氯化钡溶液 | a |
| ③ | CO | CO2 | 氢氧化钠溶液 | c |
| ④ | CaO | CaCO3 | 不用试剂 | d |
