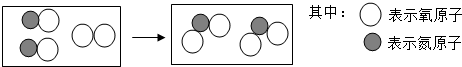
题目内容
镁是叶绿素中唯一的金属元素,植物缺镁时,通常的症状表现为叶片失绿,严重时整片叶干枯.给农作物施加 MgSO4和NH4MgPO4(磷酸镁铵)等镁肥,可以促进光合作用,提高抗病能力.(后三个小题要有完整的计算过程)
(1)NH4MgPO4 中含有 种元素.
(2)NH4MgPO4的中N、H、Mg、P、O的原子个数比为 .
(3)计算NH4MgPO4的相对分子质量.
(4)计算NH4MgPO4 中 Mg和O元素的质量比.
(5)计算NH4MgPO4 中 Mg元素的质量分数( 精确到0.1%).
(1)NH4MgPO4 中含有
(2)NH4MgPO4的中N、H、Mg、P、O的原子个数比为
(3)计算NH4MgPO4的相对分子质量.
(4)计算NH4MgPO4 中 Mg和O元素的质量比.
(5)计算NH4MgPO4 中 Mg元素的质量分数( 精确到0.1%).
考点:化学式的书写及意义,相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算
专题:化学用语和质量守恒定律
分析:(1)根据磷酸镁铵化学式的含义进行分析解答.
(2)根据1个磷酸镁铵分子的构成进行分析解答.
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(4)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(5)根据化合物中元素的质量分数=
×100%,进行分析解答.
(2)根据1个磷酸镁铵分子的构成进行分析解答.
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(4)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(5)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
解答:解:(1)磷酸镁铵是由氮、氢、镁、磷、氧五种元素组成的.
(2)1个磷酸镁铵分子是由1个氮原子、4个氢原子、1个镁原子、1个磷原子和4个氧原子构成的,则N、H、Mg、P、O的原子个数比为1:4:1:1:4.
(3)NH4MgPO4的相对分子质量14+1×4+24+31+16×4=137.
(4)NH4MgPO4中Mg和O元素的质量比为24:(16×4)=3:8.
(5)算NH4MgPO4中Mg元素的质量分数为
×100%≈17.5%.
故答案为:(1)五;(2)1:4:1:1:4;(3)137;(4)3:8;(5)17.5%.
(2)1个磷酸镁铵分子是由1个氮原子、4个氢原子、1个镁原子、1个磷原子和4个氧原子构成的,则N、H、Mg、P、O的原子个数比为1:4:1:1:4.
(3)NH4MgPO4的相对分子质量14+1×4+24+31+16×4=137.
(4)NH4MgPO4中Mg和O元素的质量比为24:(16×4)=3:8.
(5)算NH4MgPO4中Mg元素的质量分数为
| 24 |
| 137 |
故答案为:(1)五;(2)1:4:1:1:4;(3)137;(4)3:8;(5)17.5%.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
水是生命之源,也是重要的溶剂.下列有关水的说法正确的是( )
| A、水电解生成氢气和氧气,说明水中含有氢分子和氧分子 |
| B、用肥皂水可以区分硬水和软水 |
| C、净化水的常用方法有沉淀、过滤、吸附、蒸馏等 |
| D、水体有一定的自净功能,部分工业污水可直接排放 |
下列各组物质的溶液不用其他试剂就可鉴别的是( )
| A、HCl CuCl2 NaNO3 Na2SO4 |
| B、BaCl2 Na2CO3 HCl (NH4)2CO3 |
| C、FeCl3 HCl NaCl NaOH |
| D、Na2CO3 Na2SO4 HCl HNO3 |
2010年4月玉树地震后,防疫人员使用各种消毒剂对环境进行消毒.亚氯酸钠(NaClO2)是一种重要的消毒剂.下列说法不正确的是( )
| A、闻到消毒剂气味是因为微粒在不断运动 |
| B、NaClO2是由NaCl和O2构成的 |
| C、NaClO2中含量最多的元素是氯元素 |
| D、NaClO2中氯元素的化合价为+3 |
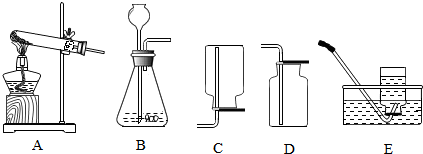
 下列几种气体可用如图所示装置干燥、收集的正确组合是( )
下列几种气体可用如图所示装置干燥、收集的正确组合是( )