题目内容
1.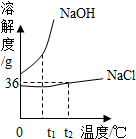 如图是氯化钠、氢氧化钠两种固体物质的溶解度曲线.
如图是氯化钠、氢氧化钠两种固体物质的溶解度曲线.①t1℃时,NaOH饱和溶液的溶质质量分数NaCl饱和溶液的溶质质量分数大于(填“大于”、“小于”、“等于”之一)
②t2℃时,将 20gNaCl固体投入50g水中,充分溶解后可得到NaCl的饱和溶液(填“不饱和溶液”或“饱和溶液”之一),此时所得溶液的质量是68g.
分析 (1)饱和溶液的溶质质量分数与该温度下的溶质的溶解度有关.
(2)根据该温度下氯化钠的溶解度分析所加物质能否完全溶解,进而判断溶液是否饱和.
解答 解:(1)由曲线图可知,t1℃时NaOH的溶解度大于NaCl的溶解度,则该温度下,两种物质的饱和溶液的溶质质量分数大小关系为:NaOH>NaCl.
故填:大于;
(2)t2℃时,NaCl的溶解度是36g,因此将20gNaCl固体投入50g水中,充分溶解后可得到NaCl的饱和溶液,此时所得溶液的质量=50g+18g=68g;
故填:饱和溶液;68;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算、饱和溶液与不饱和溶液之间的转化等,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
11.下列物质及其主要成分表示正确的是( )
| A. | 磁铁矿:主要成分是Fe2O3 | B. | 赤铁矿:主要成分是Fe2O3 | ||
| C. | 菱铁矿:主要成分是FeO | D. | 铁锈:主要成分是Fe3O4 |
12.小刚同学在学习了酶的知识后联系生活中重金属中毒事件,又提出了自己的一个猜想:酶的催化作用可能会受到重金属离子的影响.结合猜想小刚进行了如下探究:
【查阅资料】铜属于重金属,钠不是重金属.
【设计实验】取试管4支,编号,按表分别加入试剂,摇匀,迅速置于37℃的水浴中,10分钟后取出,冷却后分别加入碘液3滴,观察其颜色变化.
【实验结论】酶的催化作用受到重金属离子的影响.
【分析与交流】
(1)小刚同学提出猜想的依据是:酶是一种蛋白质,遇到重金属离子会变性.(填“糖类”、“脂肪”、“蛋白质”).
(2)在看了小刚的设计及实验后,同桌的小王认为凭上述实验还不足以证明小刚的猜想.你认为下列甲、乙、丙、丁四种改进方案是可行的有:甲乙
甲:将硫酸铜溶液更换成氯化铜溶液乙:将氯化钠溶液更换成硫酸钠溶液
丙:将硫酸铜溶液更换成硝酸铜溶液丁:将氯化钠溶液更换成硝酸钠溶液
(3)在生活中重金属盐类通常也被作为消毒杀菌的药物来使用,你能用所学的知识解释:为什么可以用0.9%的生理盐水来减轻硝酸银的腐蚀性?NaCl+AgNO3═AgCl↓+NaNO3(用化学方程式表示)
【查阅资料】铜属于重金属,钠不是重金属.
【设计实验】取试管4支,编号,按表分别加入试剂,摇匀,迅速置于37℃的水浴中,10分钟后取出,冷却后分别加入碘液3滴,观察其颜色变化.
| 编号 | 0.25%淀粉溶液(ml) | 蒸馏水(ml) | 0.9%NaCl溶液(ml) | 0.9%CuSO4溶液(ml) | 唾液溶液(ml) | 加入碘液3滴后现象 |
| 1 | 3 | 2 | - | - | - | 变蓝色 |
| 2 | 3 | 1 | - | - | 1 | 不变蓝 |
| 3 | 3 | - | 1 | - | 1 | 不变蓝 |
| 4 | 3 | - | - | 1 | 1 | 变蓝色 |
【分析与交流】
(1)小刚同学提出猜想的依据是:酶是一种蛋白质,遇到重金属离子会变性.(填“糖类”、“脂肪”、“蛋白质”).
(2)在看了小刚的设计及实验后,同桌的小王认为凭上述实验还不足以证明小刚的猜想.你认为下列甲、乙、丙、丁四种改进方案是可行的有:甲乙
甲:将硫酸铜溶液更换成氯化铜溶液乙:将氯化钠溶液更换成硫酸钠溶液
丙:将硫酸铜溶液更换成硝酸铜溶液丁:将氯化钠溶液更换成硝酸钠溶液
(3)在生活中重金属盐类通常也被作为消毒杀菌的药物来使用,你能用所学的知识解释:为什么可以用0.9%的生理盐水来减轻硝酸银的腐蚀性?NaCl+AgNO3═AgCl↓+NaNO3(用化学方程式表示)
9.张三同学在一次预习中对下列实验现象进行分析,你认为其结论正确的是( )
| A. | 某无色溶液滴入酚酞试液显红色,该溶液不一定是碱溶液 | |
| B. | 某固体加入稀盐酸,产生无色气体,证明该固体一定含有CO32- | |
| C. | 某溶液中滴加BaCl2溶液,产生不溶于稀HNO3的白色沉淀,该溶液中一定含有SO42- | |
| D. | 验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH?,再加AgNO3溶液,有白色沉淀出现,证明含有Cl- |
13.将CO和CO2的混合气体2.4g通过足量的灼热的氧化铜,完全反应后,得到CO2的质量为3.2g,则( )
| A. | 参加反应的CO为0.8g | |
| B. | 原混合气体中CO和CO2的质量比为7:5 | |
| C. | 反应完全后可得到铜6.4g | |
| D. | 该反应还可以用来除去CO中混有的CO2气体 |
10.按下列装置实验,不能达到对应目的是( )
| A. | 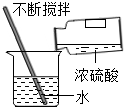 浓硫酸稀释 | B. | 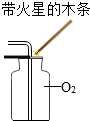 O2验满 | ||
| C. | 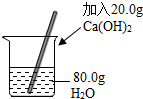 配制20%的Ca(OH)2溶液 | D. | 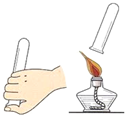 氢气验纯 |