题目内容
13.早在春秋战国时期,我国就开始生产和使用铁器.铁矿石冶炼成铁是一个复杂的过程.
(1)在实验室里,可以利用图A、B两套装置将氧化铁还原成铁;
①装置A中,木炭和氧化铁反应的化学方程式为3C+2Fe2O3 $\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑;
澄清石灰水中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
②装置B中,应先通一氧化碳(选填“通一氧化碳”或“加热氧化铁”);装置末端的酒精灯的作用为能将一氧化碳转化为无毒的二氧化碳.
(2)图C是教材中炼铁高炉及炉内化学变化过程示意图:
①若采用的铁矿石主要成分为氧化铁,请写出B区所发生主要反应的化学方程式:
B区:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
②为什么乙图中出铁口低于炉渣出口?因为生铁密度大于炉渣密度.
分析 (1)①木炭具有还原性可以将氧化铁还原成铁,同时生成二氧化碳;二氧化碳能使澄清的石灰水变浑浊;
②一氧化碳不但具有还原性,还具有可燃性,当混有了空气时在加热或是点燃的条件下容易发生爆炸,所以实验前应该先通入一氧化碳,一氧化碳有毒,排到空气中会污染空气,可以据此解答该题;
(2)①依据A区主要是生成铁而B区主要是产生一氧化碳的情况书写即可;
②结合生铁与炉渣的密度分析即可.
解答 解:(1)①木炭具有还原性可以将氧化铁还原成铁,同时生成二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水;故填:3C+2Fe2O3 $\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑,CO2+Ca(OH)2═CaCO3↓+H2O;
②一氧化碳不但具有还原性,还具有可燃性,当混有了空气时在加热或是点燃的条件下容易发生爆炸,所以实验前应该先通入一氧化碳;一氧化碳有毒,排到空气中会污染空气,装置末端的酒精灯能将一氧化碳转化为无毒的二氧化碳;故填:通一氧化碳;能将一氧化碳转化为无毒的二氧化碳;
(2)①依据A区主要是生成铁的反应,所以方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;而B区主要是产生一氧化碳共发生了两个反应,方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;故填:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
②因为生铁密度大于炉渣密度,所以乙图中出铁口低于炉渣出口;故答案为:因为生铁密度大于炉渣密度.
点评 本题主要考查了一氧化碳还原氧化铁、其高炉炼铁等方面的内容;实验室中用一氧化碳还原氧化铁制铁的过程中,一定要注意实验操作的先后顺序,注意实验前先通一氧化碳再点燃酒精喷灯,实验结束后先熄灭酒精喷灯再停止通一氧化碳.

| A. | 100 g水溶解了5 g食盐 | |
| B. | 100 g食盐溶液中含5 g食盐 | |
| C. | 5 g食盐溶解于100 g水中 | |
| D. | 将食盐和水按1:20的体积比配成的溶液 |
| A. | 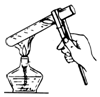 给液体加热 | B. | 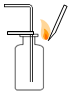 收集CO2并验满 | C. | 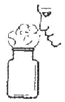 闻气体气味 | D. | 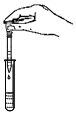 滴加液体 |
 小琪往如图所示的烧杯中加入一种物质,轻轻搅拌后,粘在烧杯上的塑料片脱落,加入的物质可能是( )
小琪往如图所示的烧杯中加入一种物质,轻轻搅拌后,粘在烧杯上的塑料片脱落,加入的物质可能是( )| A. | 食盐 | B. | 硝酸铵 | C. | 氢氧化钠固体 | D. | 冰块 |
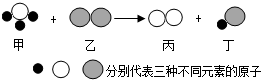 如图是某反应的微观示意图,对该图示描述错误的是( )
如图是某反应的微观示意图,对该图示描述错误的是( )| A. | 该反应前后元素的种类没变 | |
| B. | 生成物丁可能是氧化物 | |
| C. | 该反应属于分解反应 | |
| D. | 该反应中甲物质的一个分子中含有四个原子. |



