题目内容
2.铁在空气中锈蚀,实际上是铁跟氧气、水等物质作用,生成疏松多孔的铁锈,铁锈为红棕色,其主要成分是Fe2O3.磁铁矿的主要成分是四氧化三铁.分析 可以根据铁生锈的条件方面进行分析、判断,从而得出正确的结论.铁在有水和氧气并存时易生锈.
解答 解:铁在空气中锈蚀实际上是跟氧气、水等物质相互作用,发生一系列复杂的化学反应,生成疏松多孔的铁锈,铁锈为红棕色,铁锈的主要成分是 Fe2O3,它是一种疏松的物质.磁铁矿的中主要成分四氧化三铁.
故答案:氧气;水;疏松多孔;红棕;Fe2O3;四氧化三铁.
点评 本题主要考查了铁生锈的条件及其铁锈的化学式和性质等方面的知识.可以依据已有的课本知识进行.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
12.氨气变成液氨是由于( )
| A. | 分子的性质发生了变化 | B. | 分子间的间隔发生了变化 | ||
| C. | 分子组成发生了变化 | D. | 分子运动停止了 |
10.下列对质量守恒定律的理解正确的是( )
| A. | 化学反应前后分子的总数一定不会发生变化 | |
| B. | 化学反应前后元素的种类一定不会发生改变 | |
| C. | 化学反应前后物质的种类一定不会发生改变 | |
| D. | 化学反应前后原子个数可能发生改变 |
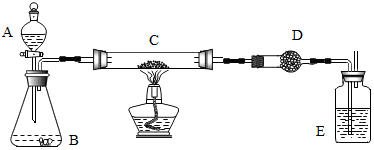
12.化学课上教师演示了加热炭粉(过量)和氧化铜混合物的实验,课后课外活动小组同学对教师演示中获得的灰红色粉末样品进行实验.实验装置如图所示(图中铁架台等装置已略去,D中盛放的是固体氢氧化钠和氧化钙的混合物).
实验主要原理:称取样品粉末W g,放入C中;D中装入ag药品;反应结束,冷却后,称量D中药品质量为b g.样品中铜的质量分数=$\frac{[w-(b-a)×\frac{12}{44}]}{w}$
请回答下列问题.
①主要实验内容
②实验讨论
装置E中盛放的试剂是澄清石灰水,其作用是检验D装置是否完全吸收了二氧化碳.
按上述实验,得到铜的质量分数不精确,你认为是偏小(填:偏大、偏小、或不能确定),原因是水蒸气通过C被D中碱石灰吸收,测得二氧化碳质量偏大,如果要得到了较正确的结果,对该装置改进的方法是在装置B与C之间接一个与D相同的装置.

实验主要原理:称取样品粉末W g,放入C中;D中装入ag药品;反应结束,冷却后,称量D中药品质量为b g.样品中铜的质量分数=$\frac{[w-(b-a)×\frac{12}{44}]}{w}$
请回答下列问题.
①主要实验内容
| 实验主要步骤 | 实验现象 | 有关化学方程式 |
| 打开A的上塞、活塞,慢慢滴加溶液 | B、E中有气泡 | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |
| 对C进行加热,当C中药品充分反应后,关闭A的活塞,停止加热 | C中的灰红色粉末变成黑色 | C+O2$\frac{\underline{\;点燃\;}}{\;}$ CO2 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO |
装置E中盛放的试剂是澄清石灰水,其作用是检验D装置是否完全吸收了二氧化碳.
按上述实验,得到铜的质量分数不精确,你认为是偏小(填:偏大、偏小、或不能确定),原因是水蒸气通过C被D中碱石灰吸收,测得二氧化碳质量偏大,如果要得到了较正确的结果,对该装置改进的方法是在装置B与C之间接一个与D相同的装置.

 碘元素是人体必需的微量元素之一.
碘元素是人体必需的微量元素之一.