题目内容
14.如表是氯化钠和硝酸钾在不同温度时的溶解度,下列说法正确的是( )| 温度/℃ | 30 | 50 | 70 | ||
| 溶解度/g | NaCl | 35.8 | 36.3 | 37.0 | 37.8 |
| KNO3 | 20.9 | 45.8 | 85.5 | 138 | |
| A. | KNO3的溶解度受温度的影响大 | |
| B. | 两者不可能有相同的溶解度 | |
| C. | 30℃时,20gKNO3与50g水混合,充分溶解后,得到饱和溶液 | |
| D. | 50℃时,NaCl的饱和溶液中溶质质量分数是37.0% |
分析 A、根据表中数据分析;B、根据溶解度数值分析考虑;C、根据30℃硝酸钾的溶解度考虑;D、根据饱和溶液溶质质量分数的计算与溶解度有关考虑.
解答 解:A、根据表中数据可知KNO3的溶解度受温度的影响大,故A说法正确;
B、根据溶解度数值分析可知,温度小于30℃,溶解度可能相等,故B说法错误;
C、30℃硝酸钾的溶解度是45.8g,所以在30℃,100g水中最多溶解45.8g硝酸钾,50g水中最多溶解22.9g,所以30℃时,20gKNO3与50g水混合,充分溶解后,得到不饱和溶液,故C说法错误;
D、50℃时,NaCl的饱和溶液中溶质质量分数是$\frac{37.0g}{137.0g}×100%$=27%,故D说法错误.
故选A.
点评 解答本题关键是熟悉溶解度曲线的意义,知道溶解度的四要素,饱和溶液溶质质量分数的计算方法.

练习册系列答案
相关题目
9.小王家的柑橘树结的果实偏小,叶色发黄,小王应向柑橘树施加下列化肥中的( )
| A. | 硫酸钾 | B. | 硫酸铵 | C. | 磷铵 | D. | 过磷酸钙 |
2.下列图象能正确反应其对应的实验操作的是( )
| A. | 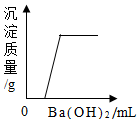 向CuCl2和H2SO4的混合溶液中加入过量的Ba(OH)2溶液 | |
| B. | 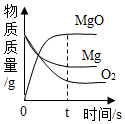 镁在氧气中燃烧 | |
| C. | 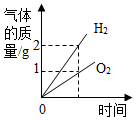 电解水得到的氢气和氧气随时间的变化 | |
| D. | 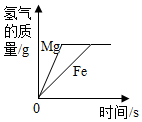 将等质量的镁粉和铁粉分别与等质量等质量分数的稀盐酸反应(固体均有剩余) |
1.如图所示的四个图象,分别对应四种过程,其中不正确的是( )
| A. | 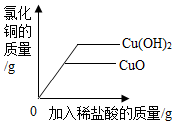 等质量的Cu(OH)2和CuO分别加入相同的稀盐酸 | |
| B. | 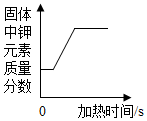 加热氯酸钾和二氧化锰的混合物制氧气 | |
| C. |  生石灰中加入一定质量的水 | |
| D. | 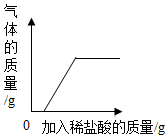 部分变质的氢氧化钠溶液中加入稀盐酸 |
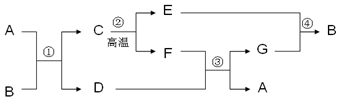

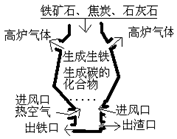 如图所示的炼铁高炉中发生了许多化学反应,其中涉及碳及其化合物的相互转化.请回答下列问题.
如图所示的炼铁高炉中发生了许多化学反应,其中涉及碳及其化合物的相互转化.请回答下列问题.