题目内容
17.N(NO2)3是科学家近年发现的一种新型火箭燃料.请计算:(1)N(NO2)3中氮、氧原子的个数比为2:3;
(2)N(NO2)3中氮、氧元素的质量比为7:12;
(3)N(NO2)3的相对分子质量是152;
(4)下列化合物中,氮元素质量分数最小的是B(填字母).
A.N2O3 B.N2O5 C.N(NO2)3.
分析 (1)根据1个N(NO2)3分子的构成进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;
(4)把每个化学式都变形成只含2个氮原子,与氮原子结合的氧原子的个数越多,氮原子的质量分数越小进行解答.
解答 解:(1)1个N(NO2)3分子中含有4个氮原子和6个氧原子,则N(NO2)3中氮、氧原子个数比是4:6=2:3.故填:2:3;
(2)N(NO2)3中氮元素和氧元素的质量比为(14×4):(16×2×3)=7:12.故填:7:12;
(3)N(NO2)3的相相对分子质量=14×4+16×6=152.故填:152;
(4)A.N2O3 B.N2O5 C.N(NO2)3--N2O3
则2个氮原子结合氧原子最多的是N2O5,
故选B.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
8.笑气是人类最早应用于医疗的麻醉剂之一,笑气的化学式为N2O,则笑气中氮元素的化合价为( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
2.用数轴表示某些化学知识直观、简明、易记.下列表示不正确的是( )
| A. | $→_{地壳中部分元素的含量}^{氧硅铝(小)}$ | |
| B. | $→_{硫元素的化合价}^{H_{2}S、S、SO_{2}、H_{2}SO_{4}(高)}$ | |
| C. | $→_{部分元素原子序数的关系}^{H、C、Na、Mg(大)}$ | |
| D. | $→_{粒子的体积关系}^{离子、原子、分子(大)}$ |
6.下列关于化学反应的实验现象描述正确的是( )
| A. | 打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾 | |
| B. | 在电解水实验中,正负两极产生的气体体积比约为2:1 | |
| C. | 木炭在空气中燃烧生成黑色有刺激性气味的气体 | |
| D. | 铁丝在氧气中剧烈燃烧,火星四射,放出大量热,生成四氧化三铁 |
7.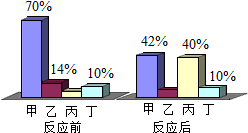 一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示.下列说法正确的是( )
一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示.下列说法正确的是( )
 一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示.下列说法正确的是( )
一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示.下列说法正确的是( )| A. | 该反应中乙、丙的质量比为3:17 | B. | 该反应中甲、丙的质量比为7:10 | ||
| C. | 该反应的基本类型为分解反应 | D. | 丁一定是该反应的催化剂 |
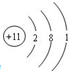 ,所以金属钠的化学性质很活泼,在空气中极易被氧化成氧化钠,用小刀一切,就露出它本来面目,银白色有金属光泽.钠还能与水反应,生成氢氧化钠(NaOH)和氢气.实验室中的金属钠通常保存在煤油中.
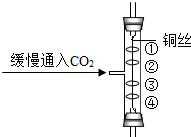
,所以金属钠的化学性质很活泼,在空气中极易被氧化成氧化钠,用小刀一切,就露出它本来面目,银白色有金属光泽.钠还能与水反应,生成氢氧化钠(NaOH)和氢气.实验室中的金属钠通常保存在煤油中.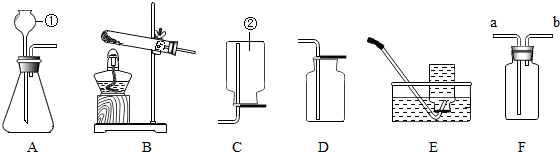
 A(填字母),若选择F装置收集H2S,气体应该从a(填“a”或“b”)端进入,实验结束后剩余的H2S气体用氢氧化钠溶液吸收,吸收的目的是防止硫化氢污染空气.
A(填字母),若选择F装置收集H2S,气体应该从a(填“a”或“b”)端进入,实验结束后剩余的H2S气体用氢氧化钠溶液吸收,吸收的目的是防止硫化氢污染空气.
 .
.