题目内容
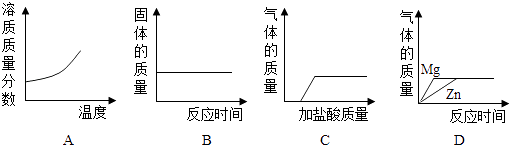
【题目】图l表示向一定量氯化钙和稀盐酸的混合溶液中滴加碳酸钠溶液,横坐标表示加入的碳酸钠溶液的质量,纵坐标表示实验中得到的沉淀或气体的质量;图2表示一定体积的气体X和不同体积的氧气反应(若反应生成水,水为液态),横坐标表示通入的氧气体积;纵坐标表示反应后气体的总体积(反应前、后的温度与压强相同.同温同压下,相同体积的任何气体含有相同的分子数). 下列叙述中正确的是( )
①图l中Oa段表示实验中沉淀质量的变化情况
②图l中c点表示上述混合溶液与碳酸钠溶液恰好完全反应
③由图2可知,反应前X的体积为2L
④由图2可知,x可能是C0或CH4 .
A.①④
B.②③
C.①②④
D.②③④
【答案】B
【解析】解:图一:根据图一可知一开始没有产生沉淀原因是加入的碳酸钠先与盐酸反应,则Oa段是气体质量的变化,当把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,则bc段即是沉淀质量的变化,达到c点沉淀量最大,氯化钙已完全反应,故①错误②正确. 图二:由图二可知反应开始气体的体积是2L即是X的体积,反应一段时间后气体的体积不会变化即气体的分子个数不变,反应完全后气体的体积随着氧气的加入不断变大,由于2CO+O2 ![]() 2CO2的反应中气体的一氧化碳分子个数是2变成2个分子,CH4+2O2
2CO2的反应中气体的一氧化碳分子个数是2变成2个分子,CH4+2O2 ![]() CO2+2H2O反应前甲烷分子的个数是1反应后气体的二氧化碳分子个数是1,两种情况都会使气体的体积均无变化.但如果是一氧化碳则氧气体积是一升时二升一氧化碳完全消耗,再加入氧气体积即会上升,与图象不符,故不正确,而甲烷则是在消耗氧气到4升时才完全反应完,再加入氧气,则混合后气体的体积才有可能上升,图象与过程符合故③正确④错误.
CO2+2H2O反应前甲烷分子的个数是1反应后气体的二氧化碳分子个数是1,两种情况都会使气体的体积均无变化.但如果是一氧化碳则氧气体积是一升时二升一氧化碳完全消耗,再加入氧气体积即会上升,与图象不符,故不正确,而甲烷则是在消耗氧气到4升时才完全反应完,再加入氧气,则混合后气体的体积才有可能上升,图象与过程符合故③正确④错误.
故选B.
【考点精析】本题主要考查了根据化学反应方程式的计算的相关知识点,需要掌握各物质间质量比=系数×相对分子质量之比才能正确解答此题.

 阅读快车系列答案
阅读快车系列答案【题目】将0.8g草酸亚铁(FeC2O4)放在一个可称量的敞口容器中加热灼烧,固体质量随温度升高而变化的数据如下(下表中所注明的各温度下,容器中的固体均为纯净物):
温度(℃) | 25 | 350 | 400 | 500 | 600 | 900 |
固体质量(g) | 0.80 | 0.80 | 0.40 | 0.44 | 0.44 | 0.43 |
下列叙述错误的是( )
①400℃时,容器中的固体为碳酸盐;
②400℃~500℃,发生了化合反应;
③600℃~900℃,发生的反应可表示为:6Fe2O3 ![]() 4Fe3O4+O2↑.
4Fe3O4+O2↑.
A.仅①
B.仅①②
C.仅①③
D.仅②③
【题目】将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 8.8 | a |
下列判断正确的是( )
A.表中a的值为2.8
B.X一定是该反应的催化剂
C.X可能含有氢元素
D.若起始时氧气的质量是14.4g,则无X生成