题目内容
16.将一定量的锌粉加入到AgNO3和Cu(NO3)2的混合溶液中,充分反应后对烧杯中的物质进行了如图两步实验探究,根据图示现象,判断实验探究①、②前烧杯中的物质成分,下列有关说法正确的是( )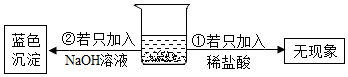
| A. | 烧杯底部固体一定只有Ag、Cu | |
| B. | 溶液的颜色可能是无色的 | |
| C. | 溶液中一定只有Cu(NO3)2、Zn(NO3)2 | |
| D. | 溶液质量一定小于加入锌粉前的溶液质量 |
分析 锌比铜活泼,铜比银活泼,将一定量的锌粉加入到AgNO3和Cu(NO3)2的混合溶液中,锌先和硝酸银反应,如果锌足量,则后和硝酸铜反应;
银、铜不能和稀盐酸反应,锌和稀盐酸反应生成氯化锌和氢气;
氢氧化钠能和硝酸铜反应生成氢氧化铜蓝色沉淀.
解答 解:A、烧杯底部固体一定有锌和硝酸银反应生成的Ag,加入氢氧化钠溶液时产生蓝色沉淀氢氧化铜,说明硝酸铜可能没有反应,也可能和锌反应后有剩余,因此固体中不一定含有Cu,该选项说法不正确;
B、加入氢氧化钠溶液时产生蓝色沉淀氢氧化铜,说明溶液中含有硝酸铜,硝酸铜溶液是蓝色溶液,因此探究①、②前烧杯中溶液一定不是无色溶液,该选项说法不正确;
C、加入稀盐酸无明显现象,说明溶液中不含有硝酸银,因此溶液中一定只有锌和硝酸银反应生成的Zn(NO3)2和没有反应或反应后剩余的Cu(NO3)2,该选项说法正确;
D、锌和硝酸银、硝酸铜反应的化学方程式及其质量关系为:
Zn+2AgNO3=Zn(NO3)2+2Ag,Zn+Cu(NO3)2=Zn(NO3)2+Cu,
65 216 65 64
由以上反应可知,锌和硝酸银反应后溶液质量减小,锌和硝酸铜反应后溶液质量增大,当硝酸铜含量很大、硝酸银含量很小时,溶液质量可能大于加入锌粉前的溶液质量,该选项说法不正确.
故选:C.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
6.下列有关物质的鉴别方法,其中不正确的是( )
| A. | 用二氧化锰鉴别水和双氧水 | |
| B. | 观察颜色、闻气味鉴别软水和硬水 | |
| C. | 灼烧闻气味鉴别羊毛和尼龙 | |
| D. | 用水鉴别氢氧化钠和氯化钠两种白色固体 |
7.下列实验现象描述正确的是( )
| A. | 点燃纯棉纤维能闻到烧焦羽毛气味 | |
| B. | 铜片投入到稀硫酸中产生大量的气泡 | |
| C. | 硫在空气中燃烧产生淡蓝色火焰,并生成有刺激性气味的气体 | |
| D. | 打开盛有浓盐酸的试剂瓶盖,瓶口有白烟 |
1.下列说法正确的是( )
| A. | 化合反应是指由两种物质生成一种物质的反应 | |
| B. | 物质与氧气发生的反应属于氧化反应 | |
| C. | 凡是在空气中不能燃烧的物质,在纯氧中也不能燃烧 | |
| D. | 氧化反应未必是化合反应,而化合反应必定是氧化反应 |
8.下列各组物质中,前者属于混合物、后者属于单质的是( )
| A. | 糖水 氧气 | B. | 蒸馏水 氮气 | ||
| C. | 氯化钠溶液 空气 | D. | 二氧化碳 氢气 |
5.中国著名的化工专家侯德榜先生通过“联合制碱法”制得的“碱”是( )
| A. | Na2CO3 | B. | NaOH | C. | Ca(OH)2 | D. | NaCl |
 (1)用数字和符号表示:①2个氧原子2O,②氧化亚铁中铁元素显+2价$\stackrel{+2}{Fe}$O.
(1)用数字和符号表示:①2个氧原子2O,②氧化亚铁中铁元素显+2价$\stackrel{+2}{Fe}$O.