题目内容
10g氢气和氧气的混合气体在一密闭容器中点燃后共生成9g水,则密闭容器中氢气和氧气
A、1:8 B、2:8 C、9:1 D、 .
A、1:8 B、2:8 C、9:1 D、
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据氢气在氧气中燃烧的化学方程式,由生成水的质量,计算出参加反应的氢气和氧气的质量,进行分析解答即可.
解答:解:设参加反应的氢气和氧气的质量分别为x、y
2H2+O2
2H2O
4 32 36
x y 9g
=
x=1g
=
y=8g
若反应后氢气有剩余,则密闭容器中氢气和氧气的质量比为(1g+1g):8g=2:8.
若反应后氧气有剩余,则密闭容器中氢气和氧气的质量比为1g:(8g+1g)=1:9.
故答案为:B;1:9.
2H2+O2
| ||
4 32 36
x y 9g
| 4 |
| 36 |
| x |
| 9g |
| 32 |
| 36 |
| y |
| 9g |
若反应后氢气有剩余,则密闭容器中氢气和氧气的质量比为(1g+1g):8g=2:8.
若反应后氧气有剩余,则密闭容器中氢气和氧气的质量比为1g:(8g+1g)=1:9.
故答案为:B;1:9.
点评:本题难度不是很大,考查学生利用化学反应方程式的计算来分析混合物的成分,利用化学反应判断恰好完全反应的量是正确解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
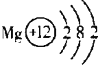 已知镁元素的原子结构示意图如图.请回答:
已知镁元素的原子结构示意图如图.请回答: