题目内容
13.同学们利用如图所示装置进行气体的制备实验(A~E为装置编号).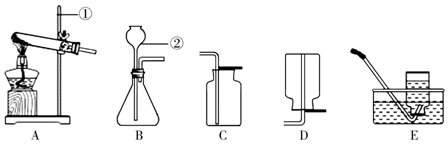
(1)写出图中标示的仪器名称:①铁架台,②长颈漏斗.
(2)实验室用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,可选用的发生装置是A.
(3)实验室用锌粒和稀盐酸制取氢气的化学方程式为Zn+2HCl=ZnCl2+H2↑.
分析 (1)根据常见的化学仪器的名称,进行分析解答.
(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,属于固体加热型制取气体,据此确定发生装置.
(3)锌粒和稀盐酸反应生成氯化锌和氢气,进行分析解答.
解答 解:(1)仪器①是铁架台;仪器②是长颈漏斗.
(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.属于固体加热型,应该选用的发生装置是A.
(3)锌粒和稀盐酸反应生成氯化锌和氢气,反应的化学方程式为Zn+2HCl=ZnCl2+H2↑.
故答案为:(1)铁架台;长颈漏斗;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑; A;
(3)Zn+2HCl=ZnCl2+H2↑.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
13.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g平均分成4份进行实验,结果如下:
(1)上表中m的数值是4.4.
(2)反应中矿石有剩余是第3、4次实验.
(3)所用稀盐酸的溶质质量分数是多少?
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成的CO2质量/g | 1.76 | 3.52 | 4.4 | m |
(2)反应中矿石有剩余是第3、4次实验.
(3)所用稀盐酸的溶质质量分数是多少?
4.下列关于“一定”的说法中,正确的是( )
| A. | 氧化物一定是化合物 | |
| B. | 非金属氧化物一定可与氢氧化钠溶液反应 | |
| C. | 如果某物质不溶于水,则一定不能和其他物质发生复分解反应 | |
| D. | 由同种元素组成的物质一定是单质 |
8.临近中考,家长为了给孩子增加营养,制定了如下食谱:
从营养均衡的角度考虑,你认为家长应该增加的食物是( )
| 主食 | 馒头、米饭、小米粥 |
| 副食 | 红烧牛肉、水煮鱼 |
| 饮料 | 酸牛奶、白开水 |
| A. | 烤面包 | B. | 炒蔬菜 | C. | 炖豆腐 | D. | 水煮虾 |
18.原子的核电荷数小于18的某元素x,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数是2n2-l.下列有关x的说法中不正确的是( )
| A. | X可能形成化学式为KXO3的含氧酸钾盐 | |
| B. | X能形成化学式为X(OH)3的碱 | |
| C. | X原子的最外层电子数和核电荷数肯定为奇数 | |
| D. | X能与某些金属元素形成化合物 |
