题目内容
3.将15g含杂质的锌粒放入盛有100g稀硫酸溶液的烧杯中,恰好完全反应后,称得烧杯内的物质的总质量为114.6g.请计算:(1)生成氢气的质量是多少克?
(2)该稀硫酸溶液中溶质的质量分数是多少?
分析 根据题干提供的信息结合质量守恒定律即可求出氢气的质量,然后根绝反应的化学方程式进行计算即可.
解答 解:(1)根据质量守恒定律,生成氢气的质量=15g+100g-114.6g=0.4g
(2)设硫酸溶液中溶质的质量为x.
Zn+H2SO4=ZnSO4+H2↑
98 2
x 0.4g
$\frac{98}{x}=\frac{2}{0.4g}$
x=19.6g
硫酸溶液的溶质质量分数=$\frac{19.6g}{100g}×$100%=19.6%
答案:
(1)生成氢气的质量是0.4g;
(2)该稀硫酸溶液中溶质的质量分数是19.6%.
点评 本题考查的是根据化学方程式的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
13.随着科技的发展和社会的进步,汽车已进入寻常百姓家.
(1)在汽车发动机后安装三效转换器可将汽车尾气中有毒气体转化为无毒气体,如图是该化学反应的微观过程模拟图,反应的化学方程式为:2NO2+4CO$\frac{\underline{\;催化剂\;}}{\;}$4CO2+N2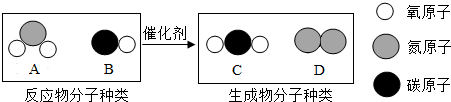
(2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,现测得反应前后各物质的质量如表:
表中x的值为14,经过测定W中含有碳、氧两种元素,且质量比为3:4,其化学式为CO.
(1)在汽车发动机后安装三效转换器可将汽车尾气中有毒气体转化为无毒气体,如图是该化学反应的微观过程模拟图,反应的化学方程式为:2NO2+4CO$\frac{\underline{\;催化剂\;}}{\;}$4CO2+N2

(2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,现测得反应前后各物质的质量如表:
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | w |
| 反应前质量/g | 23 | 40 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 22 | 27 | x |
11.下列物质的名称、俗名、化学式对应正确的是( )
| A. | 乙醇 酒精 C2H5OH | B. | 氧气 臭氧 O3 | ||
| C. | 氢氧化钠 烧碱 Na2CO3 | D. | 氢氧化钙 生石灰 Ca(OH)2 |
8.在实验室用高锰酸钾制氧气的实验中,必需的仪器是( )
| A. |  烧杯 | B. |  蒸发皿 | C. |  石棉网 | D. |  试管 |
12.质量守恒定律成立的原因是( )
①原子的数目没有增减 ②原子的种类没有改变
③化学反应前后物质总质量相等 ④原子的质量没有改变.
①原子的数目没有增减 ②原子的种类没有改变
③化学反应前后物质总质量相等 ④原子的质量没有改变.
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①②③④ |
13.下列事实能用同一原理进行解释的是( )
| A. | 金和铝在空气中都不易被腐蚀 | |
| B. | 实验室收集CO2和O2都能用向上排空气法 | |
| C. | 用嘴吹或用烧杯扣的方法,都能使燃着的蜡烛熄灭 | |
| D. | 在滴有酚酞的NaOH溶液中滴加盐酸或投入活性炭都能使溶液褪色 |