题目内容
9.科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为 4NH3+3O2$\frac{\underline{\;\;△\;\;}}{\;}$2X+6H2O,则X的化学式为( )| A. | N2 | B. | O3 | C. | H2 | D. | NO2 |
分析 根据质量守恒定律,反应前后原子的种类和数目都不变,因此可知X的化学式.
解答 解:根据化学方程式4NH3+3O2$\frac{\underline{\;\;△\;\;}}{\;}$2X+6H2O可知,反应前N原子4个,H原子12个,O原子6个;反应后H原子12个,O原子6个;则可知每个X中含有2个氮原子,则X的化学式为N2.
故选A.
点评 本题难度不大,利用化学反应前后原子守恒来确定物质的化学式是正确解答此类题的关键.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
19.从下列图片中不能获取的信息是( )


| A. | 分子之间有间隔 | |
| B. | 构成物质的粒子有分子、原子和离子 | |
| C. | 硅原子是由原子核和电子构成的 | |
| D. | 受热水分子运动速率加快 |
14.下列说法正确的是( )
| A. | 过氧化氢溶液中加入二氧化锰粉末后反应速率加快,所以催化剂就是能加快反应速率,而本身质量和化学性质不变的物质.、 | |
| B. | 2克水加热后变成2克水蒸气,变化前后质量相等,所以符合质量守恒定律 | |
| C. | 碳在高温下能使金属氧化物还原,所以碳能用于冶金 | |
| D. | 在金属活动性顺序表中,位置越前化学活动性越强,所以前面的金属必定能把位于后面的金属从它的溶液中置换出来 |
1.空气中含量较多且化学性质比较活泼的气体是( )
| A. | O2 | B. | N2 | C. | 稀有气体 | D. | CO2 |
18.如图为A、B两种固体物质随温度变化的溶解度曲线图,下列说法正确的是( )
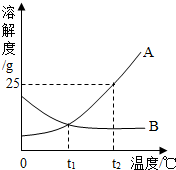

| A. | A的溶解度大于B的溶解度 | |
| B. | t2℃时等质量的水分别溶解A、B两物质达到饱和溶液时,溶质A的质量小于溶质B的质量 | |
| C. | 在其他条件不变的情况下,将A的饱和溶液的温度从t1℃升高到t2℃,有固体析出 | |
| D. | 将这两种物质的饱和溶液的温度分别从t2℃降到t1℃,A溶液的溶质质量分数大于B溶液的溶质质量分数 |
19.下列说法正确的是( )
| A. | 酒精、天然气和石油是化石燃料 | |
| B. | 变霉大米,不能食用或煮熟后食用 | |
| C. | 施用农药造成污染,应禁止使用 | |
| D. | 少食蔬菜水果的同学会缺维生素C,有可能引起坏血病 |
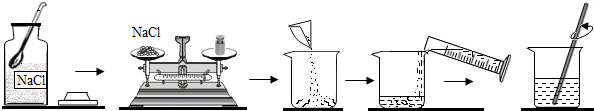
 生活中处处有化学.
生活中处处有化学.