题目内容
16.白醋无色透明,是一种能增强食品酸味的调味剂,主要成分为醋酸,与我们生活密切相联.根据所学知识回答:(1)白醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO-和H+(填离子符号);
(2)厨房中能鉴别白醋与白酒的方法有BC;A.看外观 B.闻气味 C.尝味道
(3)鸡蛋壳中含碳酸钙,白醋能软化鸡蛋壳,已知醋酸与氢氧化钙反应的方程式为:2CH3COOH+Ca(OH)2═(CH3COO)2Ca+2H2O,则醋酸与蛋壳反应的化学方程式为2CH3COOH+CaCO3═Ca(CH3COO)2+H2O+CO2↑.
分析 (1)根据醋酸电离得到醋酸根离子和氢离子进行分析;
(2)根据醋酸有酸味,白酒有芳香气味进行分析;
(3)根据醋酸和碳酸钙反应生成醋酸钙、水和二氧化碳进行分析.
解答 解:(1)醋酸电离得到醋酸根离子和氢离子;
(2)醋酸有酸味,白酒有芳香气味,所以厨房中能鉴别白醋与白酒的方法有闻气味,尝味道;
(3)醋酸和碳酸钙反应生成醋酸钙、水和二氧化碳,化学方程式为:2CH3COOH+CaCO3═Ca(CH3COO)2+H2O+CO2↑.
故答案为:(1)H+;
(2)BC;
(3)2CH3COOH+CaCO3═Ca(CH3COO)2+H2O+CO2↑.
点评 解答本题关键是要知道酸在解离时能解离出氢离子和酸根离子,知道化学式的书写方法,熟悉方程式的书写方法.

练习册系列答案
相关题目
6.a、b 两种物质的溶解度曲线如图所示.下列说法正确的是( )
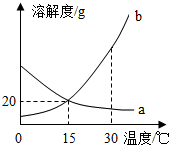

| A. | a、b 的溶解度均为20g | |
| B. | 加水或降温均可使b的饱和溶液变为不饱和溶液 | |
| C. | 30℃时,将a溶液降温至15℃,溶质的质量分数一定变小 | |
| D. | 分别向100g 水中加入a和 b的混合物20g,升温至30℃,所得a溶液可能为不饱和溶液 |
11.下列方程式符合客观事实,书写正确的是( )
| A. | 2AgNO3+Cu═Cu(NO3)2+2Ag | B. | H2SO4+Ba(OH)2═BaSO4+H2O | ||
| C. | 2Fe+6HCl═2FeCl3+3H2O | D. | KCl+HNO3═KNO3+HCl |
8.下列关于物质或粒子的说法部不正确的是( )
| A. | 丙烷(符号为C3H8)是由丙烷分子构成的 | |
| B. | 每个二氧化硫分子是由一个硫原子和两个氧原子构成的 | |
| C. | 酒精的化学式为C2H5OH,说明酒精是多原子构成的物质 | |
| D. | 最小的两个汉字“中国”是通过移动硅原子构成的文字,说明硅是由硅原子构成的 |
5.下列关于碳的性质的叙述中正确的是( )
| A. | 碳单质不都是黑色的固体 | |
| B. | 碳在高温下只能还原金属氧化物 | |
| C. | 碳的化学性质很活泼,易与空气中的氧气反应 | |
| D. | 碳和氧气在点燃条件下反应,生成CO时需要吸收热量 |
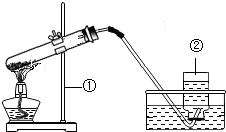 如图是实验室用氯酸钾和二氧化锰制取和收集氧气的装置,回答下列问题:
如图是实验室用氯酸钾和二氧化锰制取和收集氧气的装置,回答下列问题: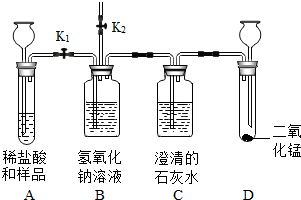 现有一份由碳酸钠和氯化钠组成的固体样品.初三化学兴趣小组的同学设计了图中的装置,请你与他们一起探究.
现有一份由碳酸钠和氯化钠组成的固体样品.初三化学兴趣小组的同学设计了图中的装置,请你与他们一起探究.