题目内容
12.在宏观、微观和符号之间建立联系是化学学科的特点,对物质进行分类是化学研究的重要方法.现有物质 ①氯化钠 ②铁 ③硝酸铵 ④水 ⑤可燃冰,请按要求填写:由分子构成的纯净物是④(填写序号),属于盐的是①③(填写序号),属于单质的是Fe(填写化学式),③中含有的阳离子是NH4+(填写符号).
分析 根据金属、大多数固态非金属单质、稀有气体等由原子构成;盐是由金属离子(或铵根离子)和酸根离子组成的化合物;单质是由一种元素组成;据此进行分析解答.
解答 解:水是由水分子构成;氯化钠属于盐,硝酸铵属于盐;铁是由铁元素组成,属于单质;硝酸铵中的阳离子是NH4+
故答案为:④;①③;Fe;NH4+
点评 本题难度不大,掌握由原子直接构成的物质(金属、大多数固态非金属单质、稀有气体等)、单质是由一种元素组成..

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.下列实验中利用提供的方案不能达到目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去铁粉中混有的少量银粉 | 用足量的稀盐酸溶解后过滤 |
| B | 除去二氧化碳中的少量一氧化碳 | 通过灼热的氧化铜 |
| C | 证明分子在不断运动 | 将一滴红墨水滴入一杯纯净水中 |
| D | 收集二氧化碳时,检验集气瓶是否集满 | 用一根燃着的木条放在集气瓶口 |
| A. | A | B. | B | C. | C | D. | D |
17.对氢氧化铜的再探究:同学们想探究能使氢氧化铜分解的最低温度到底是多少呢?于是他们又做了如下实验,采用了水浴加热,优点是能够均匀受热.分别取2毫升10%氢氧化钠溶液和1毫升10%硫酸铜溶液混合于试管中生成蓝色沉淀后,将试管置于10℃、20℃、30℃、40℃、50℃、60℃、70℃、80℃、90℃的水中进行水浴观察实验现象,并将实验结果记录如下:
(1)由以上实验可知,温度越高,氢氧化铜分解速率越快.
(2)由实验可知,氢氧化铜分解的最低温度应该在20℃~30℃之间.
(3)采取“半值法”能减少实验次数.
以上实验若按“半值法”进行,就可以省略60℃、70℃、80℃和90℃(填温度数值)的实验.
(4)实验结束后,细心的甲同学发现他的试管中剩余的浊液未经加热,已经大部分变成了黑色.由此,他想到氢氧化铜不需加热,常温下也会缓慢分解.
| 产物变化情况 | 水浴温度 | ||||||||
| 0℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ | 90℃ | |
| 试管中蓝色沉淀变化情况 | 短时间内无变化 | 短时间内无变化 | 2分钟后有出现黑色沉淀 | 30秒后出现了黑色物质 | 10秒后出现了黑色物质 | 6秒后出现黑色物质 | 数秒后出现黑色物质 | 马上出现黑色物质 | 蓝色沉淀变黑更快 |
(2)由实验可知,氢氧化铜分解的最低温度应该在20℃~30℃之间.
(3)采取“半值法”能减少实验次数.
以上实验若按“半值法”进行,就可以省略60℃、70℃、80℃和90℃(填温度数值)的实验.
(4)实验结束后,细心的甲同学发现他的试管中剩余的浊液未经加热,已经大部分变成了黑色.由此,他想到氢氧化铜不需加热,常温下也会缓慢分解.
1.铝在氧气中燃烧,参加反应的Al、O2和生成的Al2O3的质量比是( )
| A. | 27:32:102 | B. | 108:96:204 | C. | 4:3:2 | D. | 27:32:59 |
2.下列物质的化学式书写正确的是( )
| A. | 氧化钾 KO | B. | 氯化铝 AlCl2 | C. | 硫酸铁 FeSO4 | D. | 锰酸钾 K2MnO4 |

 将一定质量的Cu-Zn合金粉末放到盛有100g稀硫酸的烧杯中,恰好完全反应.放出气体的质量与反应时间的关系如图所示.
将一定质量的Cu-Zn合金粉末放到盛有100g稀硫酸的烧杯中,恰好完全反应.放出气体的质量与反应时间的关系如图所示.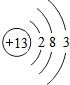 根据如图的原子结构示意图回答下列问题.
根据如图的原子结构示意图回答下列问题.