题目内容
1.在一定质量的某Na2SO4溶液中加入足量的BaCl2溶液,所得沉淀质量等于原Na2SO4溶液质量的$\frac{1}{2}$,则原Na2SO4溶液中溶质的质量分数接近于( )| A. | 10% | B. | 20% | C. | 30% | D. | 40% |
分析 根据硫酸钠和氯化钡反应生成硫酸钡沉淀和氯化钠,然后假设沉淀的质量,结合化学方程式计算出参加反应的硫酸钠的质量,再计算质量分数.
解答 解:设生成硫酸钡的质量为a克,则原硫酸钠溶液的质量为2a克,设参加反应的硫酸钠为x,
BaCl2+Na2SO4=BaSO4↓+2NaCl
142 233
x ag
$\frac{142}{x}$=$\frac{233}{ag}$
x=$\frac{142a}{233}$g
所以原Na2SO4溶液中溶质的质量分数为:$\frac{\frac{142a}{233}g}{2a}$×100%=30.5%,接近30%.
故选:C.
点评 本题主要考查了根据化学方程式的综合计算,根据反应的化学方程式可以表示反应中各物质的质量关系,由反应中某物质的质量可计算出反应中其它物质的质量.

练习册系列答案
相关题目
11.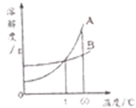 运用溶解度表与溶解度曲线回答下列问题:
运用溶解度表与溶解度曲线回答下列问题:
(1)通过对比溶解度表和溶解度曲线判断,B是氯化钠(填物质名称)的溶解度曲线.
(2)20℃时,硝酸钾和氯化钠不是属于可溶性物质(填“是”或“不是”).
(3)60℃时,l00g水中加入l00g硝酸钾,所得溶液是不饱和(填“饱和”或“不饱和”)溶液,当60℃的该溶液降温到30℃时,析出晶体的质量为54.2g.
(4)结合溶解度曲线表,试推断溶解度曲线图中t℃应在10~30℃范围内.
 运用溶解度表与溶解度曲线回答下列问题:
运用溶解度表与溶解度曲线回答下列问题:| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
(2)20℃时,硝酸钾和氯化钠不是属于可溶性物质(填“是”或“不是”).
(3)60℃时,l00g水中加入l00g硝酸钾,所得溶液是不饱和(填“饱和”或“不饱和”)溶液,当60℃的该溶液降温到30℃时,析出晶体的质量为54.2g.
(4)结合溶解度曲线表,试推断溶解度曲线图中t℃应在10~30℃范围内.
9.燃烧木柴时,通常将其劈成细条,目的是( )
| A. | 增大可燃物的热值 | B. | 增大可燃物与空气的接触面积 | ||
| C. | 提高空气中氧气的含量 | D. | 提高可燃物的着火点 |
6.在“宏观-微观-符号”之间建立联系,是化学学科特有的思维方式.如图是某化学反应的微观示意图,从中获取的相关信息正确的是( )
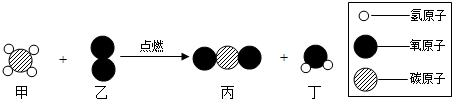

| A. | 甲物质的化学式是CH2 | B. | 丙物质属于氧化物 | ||
| C. | 该反应中有4种化合物 | D. | 甲、乙两物质的质量比为1:1 |
13.化学用语是学习化学的工具,下列化学用语与其所表示的意义相符合的是( )
| A. | Cl2-2个氯原子 | B. | Zn-1个锌分子 | C. | 2Fe-2个铁原子 | D. | 3S-3个硫元素 |