题目内容
12. 某研究小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了,且不同组实验时红色消失的时间也不同.是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
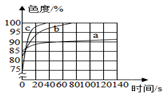
某研究小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了,且不同组实验时红色消失的时间也不同.是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?小组同学进行了实验,在a、b、c三个相同容器中分别加入等量5%、10%、20%的NaOH溶液,然后各滴加2滴酚酞试液.使用色度传感器测出溶液的颜色变化情况曲线如图.查阅资料得知,溶液无色时色度值为为100%,色度值越低颜色越深.
(1)根据上述实验操作过程,请提出你的假设:氢氧化钠溶液的浓度.
(2)另取相同容器d,加入溶质质量分数为15%且与a、b、c等量的氢氧化钠溶液,滴加2滴上述酚酞试液.你预测d容器中的溶液从出现红色到变为无色的时间可能是30s-70s之间.
(3)实验后,同学们提出“做碱使酚酞试液变红的实验时,NaOH溶液的质量分数越小越好”.你认为同学们的建议合理吗?理由是:不合理,氢氧化钠浓度太小会接近中性,遇酚酞不变色.
分析 根据氢氧化钠的浓度不同以及颜色的变化、酸碱中和反应进行分析解答即可.
解答 解:认真分析题中图可以得出:氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越大,起始颜色越深.要想进行碱与指示剂的性质实验,需要使氢氧化钠溶液的质量分数为10%较好;
(1)氢氧化钠溶液的浓度是导致滴有酚酞的NaOH溶液由红色褪为无色原因;故填:氢氧化钠溶液的浓度;
(2)氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快,10%的NaOH溶液,出现红色到变为无色的时间大约为30s,20%的NaOH溶液,出现红色到变为无色的时间大约为70s,可见15%的NaOH溶液,出现红色到变为无色的时间为30s-70s,故填:30s-70s之间;
(3)氢氧化钠浓度太小会接近中性,遇酚酞不变色,所以做碱使酚酞试液变红的实验时,NaOH溶液的质量分数越小越好不合理,故填:不合理,氢氧化钠浓度太小会接近中性,遇酚酞不变色,(或没有进行低浓度的相关实验,无法对该建议进行评价).
点评 本题考查了如何探究物质的性质和变化规律,掌握反应现象与本质的联系、学会猜想和事实验证的方法是解题的关键.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
5.下列物质中一定属于混合物的是( )
| A. | 含氮35%的硝酸铵 | B. | 含铁70%的氧化铁 | C. | 冰和水的混合物 | D. | 含碳10%的碳酸钙 |
3.“三效催化转换器”可将汽车尾气中的有毒气体转化为无污染的气体.如图所示是其中某个反应的微观示意图,下列从图示获得的信息,正确的是( )


| A. | 该图已表示出质量守恒定律 | B. | 该化学反应类型为置换反应 | ||
| C. | 甲和丁中同种元素化合价相等 | D. | 乙和丙中所含原子种类相同 |
17.下列除去杂质的方法中,正确的是( )
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | NaCl(Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
| B | CaO(CaCO3) | 加足量的水、过滤 |
| C | CaCl2(HCl) | 加足量CaCO3、过滤 |
| D | H2SO4(HCl) | 加入适量BaCl2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
4.用已知溶质质量分数的溶液可以测定未知溶液的溶质质量分数.实验室有一瓶标签模糊的稀盐酸,某同学为了测定其溶质质量分数,进行了如下实验:
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量.数据如下表:
(1)若要配制500克16%的氢氧化钠溶液,需要氢氧化钠固体80克.
(2)本次实验中,实际消耗的氢氧化钠溶液质量为25克.
(3)请通过计算确定该瓶稀盐酸的溶质质量分数.
(4)另有同学做了同样的实验,却得到了不同的结果.于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数偏大(填“偏大”或“偏小”),造成这一偏差的原因是石蕊试液的变色不明显,你能改进这个测量过程吗?请简要描述改进方案;①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴酚酞试液(质量忽略不计),重新称量;②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由无色恰好变为红色时,停止滴加,再次称量.
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量.数据如下表:
| 锥形瓶 | 锥形瓶+稀盐酸 | 锥形瓶+反应后溶液 | |
| 质量(克) | 35.5 | 55.5 | 80.5 |
(2)本次实验中,实际消耗的氢氧化钠溶液质量为25克.
(3)请通过计算确定该瓶稀盐酸的溶质质量分数.
(4)另有同学做了同样的实验,却得到了不同的结果.于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数偏大(填“偏大”或“偏小”),造成这一偏差的原因是石蕊试液的变色不明显,你能改进这个测量过程吗?请简要描述改进方案;①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴酚酞试液(质量忽略不计),重新称量;②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由无色恰好变为红色时,停止滴加,再次称量.