题目内容
 (2013?克拉玛依二模)如图是KNO3、CuSO4两种固体物质的溶解度曲线,请回答:
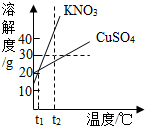
(2013?克拉玛依二模)如图是KNO3、CuSO4两种固体物质的溶解度曲线,请回答:(1)t1℃时,硝酸钾和硫酸铜的溶解度关系是
相等
相等
.(2)t2℃时,将KNO3、CuSO4两种固体各30g分别加入100g水中充分溶解,所得CuSO4溶液
是
是
(“是”或“不是”)饱和溶液,两种溶液溶质质量分数的大小关系为:m(KNO3 )>
>
m(CuSO4)(填“>”、“<”或“=”).分析:(1)根据溶解度曲线中的交点的含义考虑;(2)根据t2℃时,CuSO4的溶解度考虑;根据溶质质量分数的计算方法考虑.
解答:解:(1)曲线中交点表示该温度时两种物质的溶解度相等,所以t1℃时,硝酸钾和硫酸铜的溶解度相等;
(2)t2℃时,CuSO4的溶解度小于30g,所以t2℃时,30g硫酸铜加入100g水中充分溶解,溶液属于饱和溶液;30g溶质没有全部被溶解,t2℃时,KNO3的溶解度大于30g,所以30g溶质全部被溶解,所以硝酸钾所得溶液的溶质质量分数大,
故答案为:(1)相等;(2)是;>.
(2)t2℃时,CuSO4的溶解度小于30g,所以t2℃时,30g硫酸铜加入100g水中充分溶解,溶液属于饱和溶液;30g溶质没有全部被溶解,t2℃时,KNO3的溶解度大于30g,所以30g溶质全部被溶解,所以硝酸钾所得溶液的溶质质量分数大,
故答案为:(1)相等;(2)是;>.
点评:解答本题关键是要知道溶解度曲线中交点的含义,知道饱和溶液的判断方法,溶质质量分数的计算方法.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
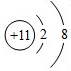 ,下列有关说法中正确的是( )
,下列有关说法中正确的是( )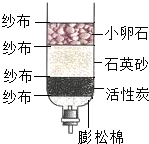 (2013?克拉玛依二模)用如图的简易净水器处理河水,下面对该净水器分析正确的是( )
(2013?克拉玛依二模)用如图的简易净水器处理河水,下面对该净水器分析正确的是( )