题目内容
9.烧杯中装有一定量的盐酸和硫酸铜的混合溶液,已知该溶液中含有HCl的质量为3.65g.某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量如下表所示:| 加入NaOH溶液的质量/g | 20.0 | 40.0 | 60.0 | 80.0 | 100.0 |
| 生成沉淀的质量/g | 0.0 | 0.00 | 2.45 | 4.90 | 4.90 |
(1)最终得到沉淀的总质量为4.90g
(2)参加反应的NaOH溶液的总质量是多少克?(结果保留小数点后面一位)
分析 氢氧化钠能和稀盐酸反应生成氯化钠和水,能和硫酸铜反应生成蓝色沉淀氢氧化铜和硫酸钠,根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断.
解答 解:(1)由表中数据可知,最终得到沉淀的总质量为4.90g.
故填:4.90.
(2)根据图表中数据可知生成4.9g沉淀不再反应了,说明最多生成4.9g沉淀;设生成4.9g沉淀参加反应的氢氧化钠的质量为x,
CuSO4+2NaOH═Cu(OH)2↓+Na2SO4,
80 98
x 4.90g
$\frac{80}{x}$=$\frac{98}{4.90g}$,
x=4.0g,
(2)设与氯化氢反应的氢氧化钠质量为y,
HCl+NaOH═NaCl+H2O,
36.5 40
3.65g y
$\frac{36.5}{3.65g}$=$\frac{40}{y}$,
y=4.0g,反应的氢氧化钠的质量总和为:4.0g+4.0g=8.0g,
参加反应的NaOH溶液的总质量是:8.0g÷10%═80.0g,
答:参加反应的NaOH溶液的总质量是80.0g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.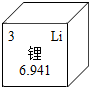 锂常被人们誉为“金属味精”,锂元素的相关信息如图,下列有关锂的说法错误的是( )
锂常被人们誉为“金属味精”,锂元素的相关信息如图,下列有关锂的说法错误的是( )
 锂常被人们誉为“金属味精”,锂元素的相关信息如图,下列有关锂的说法错误的是( )
锂常被人们誉为“金属味精”,锂元素的相关信息如图,下列有关锂的说法错误的是( )| A. | 原子的核电荷数是3 | B. | 元素符号是Li | ||
| C. | 相对原子质量为6.941 | D. | 属于非金属元素 |
20.检验一瓶久置的NaOH溶液是否变质,下列所用试剂不正确的是( )
| A. | 稀H2SO4 | B. | 酚酞试液 | C. | BaCl2溶液 | D. | Ca(NO3)2溶液 |
17.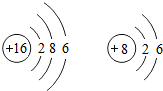 X、Y元素的原子结构示意图分别如图,下列说法中错误的是( )
X、Y元素的原子结构示意图分别如图,下列说法中错误的是( )
 X、Y元素的原子结构示意图分别如图,下列说法中错误的是( )
X、Y元素的原子结构示意图分别如图,下列说法中错误的是( )| A. | X、Y属于两种不同元素 | |
| B. | X、Y元素的化学性质相似 | |
| C. | X、Y元素在与其它元素化合时,通常显-2价 | |
| D. | X、Y元素化学性质稳定,一般不易与其它元素化合 |
4.一些食物的近似PH如表:
人的胃液中含有盐酸,对于胃酸过多的人,空腹时最宜食用上述食物中的( )
| 食 物 | 苹 果 | 葡 萄 | 牛 奶 | 玉米粥 |
| pH | 2.9-3.3 | 3.5-4.5 | 6.3-6.6 | 6.8-8.0 |
| A. | 苹果 | B. | 葡萄 | C. | 牛奶 | D. | 玉米粥 |
14.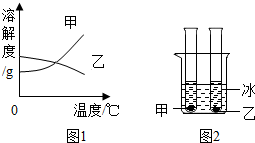 甲、乙两种固体的溶解度曲线如图1.(图2)现将两试管分别装入甲、乙两种物质室温下(20℃)的饱和溶液(试管底部均有未溶解的固体),放进盛有冰水的烧杯里,则下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图1.(图2)现将两试管分别装入甲、乙两种物质室温下(20℃)的饱和溶液(试管底部均有未溶解的固体),放进盛有冰水的烧杯里,则下列说法正确的是( )
 甲、乙两种固体的溶解度曲线如图1.(图2)现将两试管分别装入甲、乙两种物质室温下(20℃)的饱和溶液(试管底部均有未溶解的固体),放进盛有冰水的烧杯里,则下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图1.(图2)现将两试管分别装入甲、乙两种物质室温下(20℃)的饱和溶液(试管底部均有未溶解的固体),放进盛有冰水的烧杯里,则下列说法正确的是( )| A. | 甲溶液中溶质的质量分数增大 | |
| B. | 乙试管中剩余的固体减少 | |
| C. | 试管里甲、乙两物质的溶解度都增大 | |
| D. | 试管里甲、乙两溶液中的溶质都减少 |