题目内容
(1)已知一个碳原子质量为1.992×10﹣26kg,一个硫原子的质量为5.315×10﹣26kg,请根据有关知识计算:
①硫原子的相对原子质量(结果保留整数);
②若该硫原子核外电子数为16,则它的中子数是多少?
(2)硫酸钾的相对分子质量是 ,其中钾元素、硫元素、氧元素的质量比为 .
(3)请计算多少克硫酸钾中钾元素质量与14.9克氯化钾中钾元素质量相等?
考点: 相对原子质量的概念及其计算方法;原子的有关数量计算;相对分子质量的概念及其计算;元素质量比的计算;化合物中某元素的质量计算.
专题: 化学式的计算;物质的微观构成与物质的宏观组成.
分析: (1)①根据某原子的相对原子相对质量= ,结合题意进行分析解答即可.
,结合题意进行分析解答即可.
②根据相对原子质量=质子数+中子数;
(2)根据化学式的意义进行分析,相对分子质量是所有原子相对原子质量的总和,元素的质量比等于各原子相对原子质量和之比,根据元素的含量可以确定元素的质量分数,从而求出元素的质量.
(3)根据元素的质量=化合物的质量×元素的质量分数;
解答: 解:(1)①根据某原子的相对原子相对质量= ,硫原子的相对原子质量=
,硫原子的相对原子质量=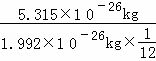 =32;
=32;
②硫原子中子数=32﹣16=16;
答案:32;16;
(2)硫酸钾的相对分子质量为:39×2+32+16×4=174;
硫酸钾中钾元素、硫元素、氧元素的质量比为:39×2:32:16×4=39:16:32;
答案:174;39:16:32;
(3)设质量为x的硫酸钾中钾元素质量与14.9克氯化钾中钾元素质量相等;
x×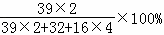 =14.9g×
=14.9g×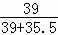
x=17.4g
答:17.4g的硫酸钾中钾元素质量与14.9克氯化钾中钾元素质量相等
点评: 本题考查了根据化学式的计算,完成此题,可以依据化学式的意义进行.

下列化学式正确的是( )
|
| A. | 高锰酸钾(K2MnO4) | B. | 氧化镁(MgO2) | C. | 氯化钾(KClO3) | D. | 氯化亚铁(FeCl2) |
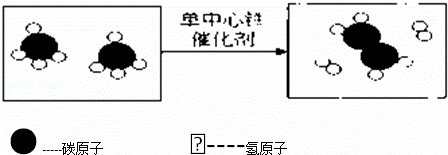
我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获重大突破.成果在最近的美国《科学》杂志发表.该转化的微观示意图如图:有关该转化的说法错误的是( )
|
| A. | 反应前后原子的种类变化 | B. | 催化剂改变了反应速率 |
|
| C. | 该反应是分解反应 | D. | 反应物与生成物均由分子构成 |
下列说法错误的是( )
|
| A. | 有气体生成的变化不一定是化学变化 |
|
| B. | 实验室剩余的药品应放回原瓶 |
|
| C. | 实验中不能品尝任何药品的味道 |
|
| D. | 烧杯可用于溶解药品,也可用作反应容器 |
有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入等质量等浓度的稀硫酸中,乙、丙表面有气泡产生,且丙产生气泡较快;再将甲投入丁的盐溶液中,甲的表面有丁析出,则这四种金属活动性顺序为( )
|
| A. | 甲>乙>丙>丁 | B. | 丙>乙>甲>丁 | C. | 丙>乙>丁>甲 | D. | 丁>甲>乙>丙 |
