题目内容
15.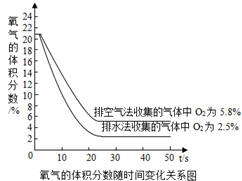 用氧气测量仪测得收集的气体中氧气的体积分数随时间的变化关系如图(起始时氧气的体积分数都以21%计),则最终两种方法收集的气体中二氧化碳体积分数较大的是排水(填“排空气”或“排水”)法,两种方法收集的气体中二氧化碳体积分数的差值是15.7%.
用氧气测量仪测得收集的气体中氧气的体积分数随时间的变化关系如图(起始时氧气的体积分数都以21%计),则最终两种方法收集的气体中二氧化碳体积分数较大的是排水(填“排空气”或“排水”)法,两种方法收集的气体中二氧化碳体积分数的差值是15.7%.
分析 用氧气测量仪测得收集的气体中氧气体积分数随时间的变化关系如图2(起始时氧气的体积分数都以21%计),则最终两种方法收集的气体中二氧化碳体积分数较大的是排水法,两种方法收集的气体中二氧化碳体积分数的差值是15.7%;
解答 解:用氧气测量仪测得收集的气体中氧气体积分数随时间的变化关系如图2(起始时氧气的体积分数都以21%计),则最终两种方法收集的气体中二氧化碳体积分数较大的是排水法,两种方法收集的气体中二氧化碳体积分数的差值是15.7%;故答案为:排水;15.7%;
点评 本考点主要考查了气体的收集装置的问题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5. 化学式在原子、分子水平上研究物质及其变化的科学.
化学式在原子、分子水平上研究物质及其变化的科学.
(1)现有下列化学式或微粒符号::①2CO、②Ca2+、③2H、④O2.其中,“2”表示2个分子的是①(填序号,下同),表示每个微粒带2个单位电荷的是②.
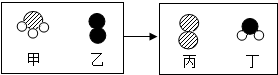
(2)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意
如图.下列说法正确的是BE(填选项).
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(3)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异.
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同);写出氢氧化镁与胃酸反应的化学方程式Mg(OH)2+2HCl=MgCl2+2H2O.
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.则铝碳酸镁起抗酸作用的两种微粒是OH-、CO32-.
 化学式在原子、分子水平上研究物质及其变化的科学.
化学式在原子、分子水平上研究物质及其变化的科学.(1)现有下列化学式或微粒符号::①2CO、②Ca2+、③2H、④O2.其中,“2”表示2个分子的是①(填序号,下同),表示每个微粒带2个单位电荷的是②.
(2)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意
如图.下列说法正确的是BE(填选项).
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(3)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2、OH-、CO32- |
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同);写出氢氧化镁与胃酸反应的化学方程式Mg(OH)2+2HCl=MgCl2+2H2O.
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.则铝碳酸镁起抗酸作用的两种微粒是OH-、CO32-.
6.已知Cl的原子结构示意图为 ,则下列说法不正确的是( )
,则下列说法不正确的是( )
 ,则下列说法不正确的是( )
,则下列说法不正确的是( )| A. | 氯原子核外有3个电子层,最外层电子数是7 | |
| B. | 氯原子核内的质子数等于氯原子核外电子总数 | |
| C. | 氯原子核的质量远大于氯原子核外电子总质量 | |
| D. | 氯原子核与核外电子所占的空间大小基本相同 |
10.下列说法不正确的是( )
| A. | 蒸发食盐水,当蒸发皿中出现较多固体时,停止加热 | |
| B. | 配制100g20%的氯化钠溶液,需要氯化钠20g | |
| C. | 溶解过程中用玻璃棒搅拌的作用是加速溶解 | |
| D. | 从100mL20%的食盐水中取出50mL,剩余溶液的溶质质量分数为10% |
19.Na2SO4、K2SO4等硫酸盐中硫元素的化合价为( )
| A. | +6 | B. | +4 | C. | 0 | D. | -2 |
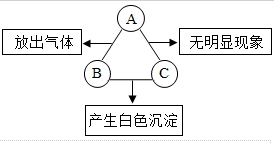 A、B、C是初中实验室常备的三种溶液,它们两两混合发生反应的现象如图所示.符合该实验现象的A、B、C三种溶液的溶质依次是盐酸、碳酸钠、氢氧化钙;若A是一种黑色粉末状单质,A与C反应溶液的颜色有变化(其他现象同图示),则B、C两种溶液的溶质的化学式依次是HCl、AgNO3.
A、B、C是初中实验室常备的三种溶液,它们两两混合发生反应的现象如图所示.符合该实验现象的A、B、C三种溶液的溶质依次是盐酸、碳酸钠、氢氧化钙;若A是一种黑色粉末状单质,A与C反应溶液的颜色有变化(其他现象同图示),则B、C两种溶液的溶质的化学式依次是HCl、AgNO3.