题目内容
有一包NaCl的固体,其中可能含有Na2CO3、CaCO3、CuSO4(无水)中的一种或两种.某化学兴趣小组的同学欲探究该固体中的成分和测定其中NaCl的质量分数,请你分析并回答下列问题:
Ⅰ.探究该固体的成分.如下图:

根据以上实验可知:
(1)由步骤①可知,该固体中一定没有 (写化学式).
(2)步骤②中分离物质的实验操作名称是 ,该步发生反应的化学方程式是 .
(3)有同学提出,不需要进行实验步骤③,也能判断出该固体成分,你认为他判断的依据是 .
Ⅱ.测定该固体中NaCl的质量分数.
另称取m g固体,加水充分溶解,再加入足量的稀硝酸,加热让反应后的气体充分逸出,然后滴加足量AgNO3溶液,产生的沉淀经过滤、洗涤、烘干,称量为n g.
(4)实验Ⅱ中加足量稀硝酸的目的是除去 (填化学式),以确保沉淀产物单一.
(5)该固体中NaCl的质量分数为 (用含m、n代数式表示).
(1)CuSO4、CaCO3
(2)过滤;Na2CO3+BaCl2═BaCO3↓+2NaCl
(3)步骤①当固体溶于水得到无色液体,因为硫酸铜溶液是蓝色的,则一定不含有硫酸铜;碳酸钙不能溶于水,则一定不含有碳酸钙;所以只可能含有碳酸钠;
(4)Na2CO3(5)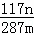 ×100%
×100%

下列事实不能用金属的活动性顺序加以解释的是( )
|
| A. | 不能用铜与稀硫酸反应制取氢气 |
|
| B. | 铁能置换出硫酸铜溶液中的铜 |
|
| C. | 在化合物中,铁显+2、+3价,铜显+1、+2价 |
|
| D. | 相同条件下,锌和铁与稀硫酸反应的剧烈程度 |
下列化学用语与含义相符的是( )
|
| A. | 2N:表示1个氮分子由2个氮原子构成 |
|
| B. | CH4:表示该物质中碳元素和氢元素的质量比为1:4 |
|
| C. | C2H5OH:表示该物质由三种元素组成,且1个分子中含9个原子 |
|
| D. | FeO:表示氧化铁 |
下列各组物质变化中,每一转化在一定的条件下均能一步实现的是( )
| X | Y | Z | |
| A | Fe | FeCl2 | Fe2O3 |
| B | CO2 | Na2CO3 | CaCO3 |
| C | H2 | H2O | H2O2 |
| D | Ca(OH)2 | NaOH | NaCl |

|
| A. | A | B. | B | C. | C | D. | D |

