题目内容
17.将铜粉和炭粉的混合物通入足量的空气加强热,充分反应后,测得剩余固体的总质量与原混合固体总质量相等,则原混合固体中铜粉和炭粉的质量比为( )| A. | 3:4 | B. | 16:3 | C. | 1:3 | D. | 4:1 |
分析 碳在空气中充分灼烧后会燃烧生成二氧化碳气体(碳粉完全消失),铜粉在空气中充分灼烧会生成氧化铜(铜粉质量增加).所以完全灼烧后的固体成分只有氧化铜.根据题意,完全灼烧后得到固体质量与原混合物相同,所以原混合物中炭粉与铜粉的质量比就等于参加反应氧气与铜粉的质量比.
解答 解:碳和铜都被完全氧化后,冷却到室温,发现固体的质量没有变化,说明碳的质量等于和铜反应的氧气的质量;
设铜的质量为x,参加反应的氧气的质量为y;
2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO
128 32
x y
$\frac{128}{x}$=$\frac{32}{y}$
所以原混合物中木炭粉与铜粉质量之比为1:4.
故选:D.
点评 本题主要考查学生利用化学方程式进行计算的能力.本题的条件比较隐蔽,解题时需根据化学方程式认真分析数量关系,才能正确解答.

练习册系列答案
相关题目
7.某同学在实验室进行了木炭还原氧化铜的实验,实验步骤如下:
⑤为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究(注:该反应还原产物只有铜).
【猜想】猜想Ⅰ:全部都是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、木炭.
【实验与结论】待试管冷却后将剩余固体倒入烧杯,加入足量稀硫酸,过滤,得到蓝色滤液,
滤渣为红色和黑色固体混合物.证明猜想猜想Ⅳ成立;写出氧化铜与稀硫酸反应的化学方程式CuO+H2SO4═CuSO4+H2O.
【实验反思】混合物中仍含有氧化铜的原因可能是碳和氧化铜没有完全反应就停止了加热,或者还可能的原因是从试管B中撤出导管时,有空气进入试管,与灼热的铜再次反应生成氧化铜.
| 实验装置 | 实验步骤 | 分析 |
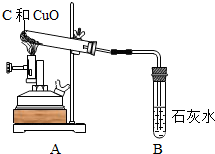 | ①检验装置气密性 | |
| ②把木炭和氧化铜的混合物放入试管,如左图所示连接实验装置 | 装置中存在的问题是B试管处不应该有橡皮塞 | |
| ③改进装置后,点燃酒精喷灯开始实验 | 装置B的作用是检验产物是否有二氧化碳 | |
| ④反应结束时,先将导管从装置B中撤出,再停止加热 | 目的是防止液体倒流引起试管炸裂 |
【猜想】猜想Ⅰ:全部都是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、木炭.
【实验与结论】待试管冷却后将剩余固体倒入烧杯,加入足量稀硫酸,过滤,得到蓝色滤液,
滤渣为红色和黑色固体混合物.证明猜想猜想Ⅳ成立;写出氧化铜与稀硫酸反应的化学方程式CuO+H2SO4═CuSO4+H2O.
【实验反思】混合物中仍含有氧化铜的原因可能是碳和氧化铜没有完全反应就停止了加热,或者还可能的原因是从试管B中撤出导管时,有空气进入试管,与灼热的铜再次反应生成氧化铜.
5.下列实验现象的描述不正确的是( )
| A. | 电解水时,正极产生氧气负极产生氢气 | |
| B. | 红磷在空气中燃烧,产生大量白烟 | |
| C. | 镁和稀盐酸反应产生无色气体,放出热量 | |
| D. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 |
2.下列实验方案中,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 分离Na2CO3和NaOH固体混合物 | 加入过量氢氧化钙溶液,过滤 |
| B | 除去NaCl固体中的少量Na2CO3 | 加入适量稀盐酸,充分反应后,蒸发 |
| C | 检验CO2气体中含有少量的CO | 将混合气体依次通过灼热的氧化铁和澄清石灰水,观察澄清石灰水的变化 |
| D | 鉴别NaCl溶液、NaOH溶液和 稀盐酸 | 各取少量溶液于试管中,分别滴加无色酚酞溶液,观察溶液颜色的变化 |
| A. | A | B. | B | C. | C | D. | D |
4.干冰用于人工降雨,当飞机喷洒干冰后,云层中不会发生变化的是( )
| A. | 水分子间的间隔 | B. | 水分子运动速率 | ||
| C. | 二氧化碳分子间间隔 | D. | 二氧化碳分子的大小 |
4.正确的操作是实验成功的前提,下列实验操作正确的是( )
| A. | 将氢氧化钠直接放在托盘天平上称重 | |
| B. | 给蒸发皿加热时,必须垫上石棉网 | |
| C. | 为了达到节约药品的目的,将实验后剩余的药品放回原瓶 | |
| D. | 洗净后试管应倒放在试管架上 |