题目内容
7.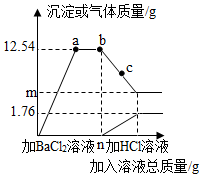 某环保小组监测到一造纸厂排放的废水中含有碳酸钠和硫酸钠两种物质,为测定废水中这两种物质的含量,环保小组的同学进行了以下实验:取该造纸厂排放的废水200g,先向其中加BaCl2溶液至ng后停止,然后再滴加稀盐酸,反应过程中加入溶液的质量与产生沉淀和气体的质量关系如图所示.
某环保小组监测到一造纸厂排放的废水中含有碳酸钠和硫酸钠两种物质,为测定废水中这两种物质的含量,环保小组的同学进行了以下实验:取该造纸厂排放的废水200g,先向其中加BaCl2溶液至ng后停止,然后再滴加稀盐酸,反应过程中加入溶液的质量与产生沉淀和气体的质量关系如图所示.(假设废水中其它成分不参与反应;钡的相对原子质量为137)
请根据图象与数据分析计算:
(1)a、b、c三点对应的溶液中所含BaCl2的质量关系是a<b<c(用“>”、“<”或“=”表示).
(2)m值等于4.66.
(3)该废水中硫酸钠的溶质质量分数(写出计算过程).
分析 氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,和硫酸钠反应生成硫酸钡沉淀和氯化钠,碳酸钡能和稀盐酸反应生成氯化钡、水和二氧化碳,硫酸钡不能和稀盐酸反应,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)由图中数据可知,a点时溶液中氯化钡质量为0,b点时溶液中氯化钡质量大于0,c点时溶液中的氯化钡质量是b点时氯化钡的质量和碳酸钡与稀盐酸反应生成的氯化钡质量只和,因此a、b、c三点对应的溶液中所含BaCl2的质量关系是 a<b<c.
故填:a<b<c.
(2)设碳酸钡质量为x,
m点时的沉淀是硫酸钡沉淀的质量,由图中信息可知,碳酸钡和稀盐酸反应生成的二氧化碳质量为1.76g,
BaCO3+2HCl═BaCl2+H2O+CO2↑,
197 44
x 1.76g
$\frac{197}{x}$=$\frac{44}{1.76g}$,
x=7.88g,
沉淀硫酸钡的质量为:12.54g-7.88g=4.66g,
因此m=4.66,
故填:4.66.
(3)设废液中硫酸钠质量为y,
BaCl2+Na2SO4═BaSO4↓+2NaCl,
142 233
y 4.66g
$\frac{142}{y}$=$\frac{233}{4.66g}$,
y=2.84g,
该废水中硫酸钠的溶质质量分数为:$\frac{2.84g}{200g}$×100%=1.42%,
答:该废水中硫酸钠的溶质质量分数为1.42%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

 阅读快车系列答案
阅读快车系列答案| A. | 可用灼烧、闻气味的方法鉴别羊毛纤维和棉纤维 | |
| B. | 用蒸馏水润湿的pH试纸测定溶液的pH,不会影响测定结果 | |
| C. | 喝下汽水后常会打嗝,说明气体的溶解度一般随温度的升高而减小 | |
| D. | 甲醛能与蛋白质发生反应,所以甲醛可用于水产品的保鲜 |

| A. | 参加反应的两种分子的个数比是1:4 | |
| B. | 无机物在一定条件下可转化为有机物 | |
| C. | 反应前后原子种类、数目均不变 | |
| D. | 该反应的化学方程式为2CO2+6H2$\frac{\underline{催化剂}}{△}$C2H4+4H2O |
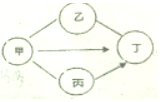
(1)若甲乙均为黑色固体,则乙一定为碳,甲一定为氧化铜
(2)若乙含有氢氧根离子,则甲一定不是碳酸钙.
(3)甲、乙、丙三种物质两两之间均可发生复分解反应
(4)若甲、乙分别为酸和碱,则丙一定是碳酸盐,
(5)丙转化为丁只能通过复分解反应实现.以上说法正确的是( )
| A. | (1)(2) | B. | (3)(4) | C. | (4)(5) | D. | (2)(3) |
| A. | I | B. | Pb | C. | Ca | D. | Zn |
| 物质 | 杂质 | 所用试剂和操作方法 | |
| A | Na2CO3溶液 | Na2SO4溶液 | 加入过量的Ba(NO3)2溶液,过滤 |
| B | H2 | HCl | 通过足量的NaOH溶液、浓硫酸 |
| C | NaCl固体 | 细沙 | 加入足量的水溶解,过滤 |
| D | 铁粉 | Fe2O3 | 加入适量的稀盐酸,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 纺纱织布 | B. | 粮食酿酒 | C. | 治炼生铁 | D. | 烧制瓷器 |
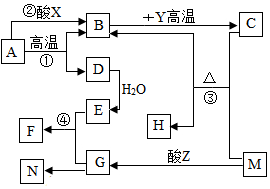 现有几种常见物质,其中D可作干燥剂,F为蓝色沉淀,M为黑色粉末,N为白色沉淀,X是实验室通常用来制取气体B的酸,Z是与X不同的酸,他们互相转化关系如图所示(部分反应物和生成物略)
现有几种常见物质,其中D可作干燥剂,F为蓝色沉淀,M为黑色粉末,N为白色沉淀,X是实验室通常用来制取气体B的酸,Z是与X不同的酸,他们互相转化关系如图所示(部分反应物和生成物略)