题目内容
1.牛奶的价格取决于蛋白质含量的高低,通用的蛋白质测试方法“凯氏定氮法”是通过测出含氮量来估算蛋白质含量.日前发现三鹿奶粉因添加三聚氰胺(C3N6H6)而产生了许多“结石”宝宝.(1)在实验室里,可以用甲醛的水溶液检验蛋白质的存在,现象是蛋白质凝固变性;
(2)三聚氰胺中碳氮氢元素的质量比为6:14:1;
(3)奶粉中添加三聚氰胺的目的是冒充蛋白质;
(4)三聚氰胺在奶粉中含量超高,但在液态奶中含量较底,是因为三聚氰胺溶解度小.三聚氰胺作为一种白色结晶粉末,没有(有、没有)气味和味道.
(5)三聚氰胺的生产是以尿素(CO(NH2)2)为原料,硅胶为催化剂,在380-400℃温度下反应生成.副产品是氨气和光合作用的一种原料.此反应的化学方程式为6CO(NH2)2$\frac{\underline{\;\;\;\;\;\;\;硅胶\;\;\;\;\;\;\;}}{380-400℃}$C3N6H6+6NH3↑+3CO2↑.
分析 (1)蛋白质的结构被破坏后,失去生理功能,这称为蛋白质的变性,能使蛋白质变性的外界条件有多种,如强酸、强碱、甲醛、酒精、重金属离子、高温、射线等.
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比解答;
(3)根据奶粉添加三聚氰胺,主要是因为它能冒充蛋白质解答;
(4)根据三聚氰胺常温下溶解度小解答;
(5)根据题意,以尿素CO(NH2)2为原料,硅胶为催化剂,在380-400℃温度下反应生成.副产品是氨气和光合作用的一种原料(二氧化碳),写出反应的化学方程式即可.
解答 解:(1)在实验室里,可以用甲醛的水溶液检验蛋白质的存在,现象是蛋白质凝固变性(合理即可).
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得三聚氰胺中C、N、H三种元素的质量比为:(12×3):(14×6):6=36:84:6=6:14:1;
(3)加入三聚氰胺提高的是奶粉中氮元素的含量,奶粉中添加三聚氰胺的目的是冒充蛋白质;
(4)三聚氰胺在奶粉中含量超高,但在液态奶中含量较底,是因为三聚氰胺溶解度小,三聚氰胺作为一种白色结晶粉末,没有气味和味道.
(5)以尿素CO(NH2)2为原料,硅胶为催化剂,在380-400℃温度下反应生成.副产品是氨气和光合作用的一种原料(二氧化碳),反应的化学方程式为:6CO(NH2)2$\frac{\underline{\;\;\;\;\;\;\;硅胶\;\;\;\;\;\;\;}}{380-400℃}$C3N6H6+6NH3↑+3CO2↑.
故答案为:
(1)甲醛的水溶液;蛋白质凝固变性;
(2)6:14:1;
(3)冒充蛋白质;
(4)小,没有;
(5)6CO(NH2)2$\frac{\underline{\;\;\;\;\;\;\;硅胶\;\;\;\;\;\;\;}}{380-400℃}$C3N6H6+6NH3↑+3CO2↑.
点评 本题难度不大,掌握蛋白质凝固变性的因素、化学方程式的书写方法是正确解答本题的关键.

| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶 解 度(g) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
| Ca(OH)2 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 | |
(2)从表中数据分析,10℃时,NaCl与KNO3的溶解度大小关系A(填序号).
A.NaCl更大 B.KNO3更大 C.两者相等 D.不能确定
(3)60℃时,将110gKNO3投入50g水充分溶解,所得溶液中溶质的质量分数为52.4%.
(4)NaCl中含有很少量KNO3杂质,为提纯NaCl,可采取的方法是:将固体恰好溶解后,蒸发至X状态,在趁热过滤,洗涤,干燥.X状态应是C(填序号)
A.剩大量水 B.剩少量水 C.有大量固体析出,看不到水 D.完全蒸干.
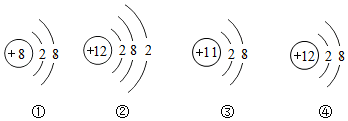
| A. | 它们表示四种不同的元素 | B. | ②在化学变化时易失两个电子 | ||
| C. | ①③④表示的元素都是非金属元素 | D. | ①④表示的是阳离子 |
 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入到该烧杯中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8克.
(2)该产品中碳酸钠的质量分数是否合格?
(要求写出计算过程,结果精确到0.1%)
(3)求所用盐酸的质量分数.(结果精确到0.1%)
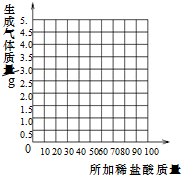
(4)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(写出必要的计算过程)
| A. | 氧气跟氧化铜反应后的残渣用硝酸清洗:Cu+2HNO3═Cu(NO3 )2+H2↑ | |
| B. | 铁跟稀盐酸反应制取氢气:2Fe+6HCl═2FeCl3+3 H2↑ | |
| C. | 石灰浆抹墙后,久置变硬:Ca(OH)2+CO2═CaCO 3↓+H2O | |
| D. | 实验室制备氧气:2H2O=2H2↑+O2↑ |
| A. | 酸碱中和 | B. | 煅烧石灰石 | ||
| C. | 铁放入硫酸铜溶液中 | D. | 生石灰与水反应 |