题目内容
17.科学家已研究出高能微粒N${\;}_{5}^{+}$,下列关于它的说法中正确的是( )| A. | N${\;}_{5}^{+}$是一种新的原子 | |
| B. | N${\;}_{5}^{+}$是由五个氮原子构成的分子 | |
| C. | N${\;}_{5}^{+}$是带一个单位正电荷的阳离子 | |
| D. | N${\;}_{5}^{+}$是带一个单位负电荷的阴离子 |
分析 根据N5+的表示方法得到它是一个带有一个单位正电荷的离子解答.
解答 解:A.由高能微粒N5+,可知是一种离子,而不是原子,故选项说法错误.
B.由高能微粒N5+,可知是一种离子,而不是分子,故选项说法错误.
C.这是一个带有一个单位正电荷的阳离子,故正确;
D.由高能微粒N5+,可知,这是一个带有一个单位正电荷的阳离子,故错误.
故选C.
点评 本题难度有一定难度,理解题意、掌握原子和离子的相互转化并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
12.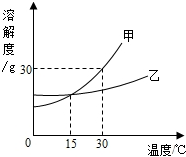 如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )
 如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )| A. | 甲的溶解度受温度影响比乙小 | |
| B. | 升高温度可使接近饱和的甲溶液变为饱和 | |
| C. | 30℃时乙的溶解度为30g | |
| D. | 15℃时甲、乙的溶解度相等 |
6.缺铁性贫血要补“铁”,骨质疏松要补“钙”,这里所说的“铁”与“钙”是指( )
| A. | 原子 | B. | 元素 | C. | 单质的铁与钙 | D. | 分子 |