题目内容
17.在工业上用纯碱和石灰石为原料制备烧碱,主要流程如图一所示:
(1)在①~④四个过程中,发生了化合反应的为②(填序号).
(2)③中实验操作过程的名称为溶解,经搅拌后,得到石灰水.
(3)NaCl、KNO3、Ca(OH)2三种物质的溶解度曲线图分别如图二、图三所示,请回答:
①由图二可知,20℃时,KNO3溶液的溶质质量分数无法确定NaCl溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一).
②由图二可知,将20℃时KNO3饱和溶液,升温到50℃时,溶液的溶质质量分数不变(填“变大”“变小”“不变”之一)
③如图四所示,20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入氢氧化钠固体,结合图三分析石灰水可出现变浑浊的现象.
分析 高温条件下,碳酸钙分解生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠;
溶液中溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%;
根据物质的溶解度曲线可以判断相关方面的问题.
解答 解:(1)在①~④四个过程中,氧化钙和水反应生成氢氧化钙,属于化合反应.
故填:②.
(2)③中实验操作过程的名称为溶解,经搅拌后,得到石灰水.
故填:溶解.
(3)①因为不知道硝酸钾和氯化钠的水溶液中的溶质质量和溶剂质量,因此20℃时,无法判断KNO3溶液的溶质质量分数和NaCl溶液的溶质质量分数的大小.
故填:无法确定.
②由图二可知,硝酸钾的溶解度随着温度升高而增大,因此将20℃时KNO3饱和溶液,升温到50℃时,溶质质量和溶液质量都不变,溶液的溶质质量分数不变.
故填:不变.
③氢氧化钙的溶解度随着温度升高而减小,20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入氢氧化钠固体,氢氧化钠溶于水放热,导致溶液温度升高,氢氧化钙的溶解度减小,溶液变浑浊.
故填:变浑浊.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
8.掌握化学用语是学好化学的关键.下列化学用语及其表述的意义合理的是( )
①H2O-1个水分子 ②2Na+-2个钠离子 ③Cl+-氯离子 ④O2-2个氧原子
⑤MgO-氧化镁 ⑥2N-2个氮元素 ⑦He2-氦气中氦元素的化合价为1.
①H2O-1个水分子 ②2Na+-2个钠离子 ③Cl+-氯离子 ④O2-2个氧原子
⑤MgO-氧化镁 ⑥2N-2个氮元素 ⑦He2-氦气中氦元素的化合价为1.
| A. | ①②③⑤ | B. | ②③④⑤ | C. | ①②⑤⑦ | D. | ②⑤⑥⑦ |
5.济南市城市轨道交通的建设时全城人民的生活、工作环境更加便捷、美丽,下列做法中,不利于改善我市环境质量的是( )
| A. | 使用清洁能源代替煤和石油 | |
| B. | 提高城市道路机扫率,增加洒水频次,控制道路扬尘 | |
| C. | 提倡使用一次性发泡塑料餐具和塑料袋 | |
| D. | 全面禁止秸秆露天焚烧,加大秸秆综合利用力度 |
12.下列各组物质的鉴别中,所选的鉴别试剂,不正确的是( )
| 选项 | 待鉴别物质 | 鉴别试剂 |
| A | 氢氧化钠溶液和氢氧化钙溶液 | 二氧化碳 |
| B | 鉴别硫酸铵和硫酸钠固体 | 氢氧化钡溶液 |
| C | 食盐溶液和稀盐酸 | 紫色石蕊 |
| D | 氮气和二氧化碳气体 | 燃着的木条 |
| A. | A | B. | B | C. | C | D. | D |
2.下列图象不能正确反映其对应变化关系的是( )
| A. |  用等质量、等浓度的 过氧化氢溶液在有无 催化剂条件下制氧气 | |
| B. |  向等质量、等浓度 的稀硫酸中分别逐 渐加入锌粉和铁粉 | |
| C. |  一定质量的红磷在 密闭容器中燃烧 | |
| D. | 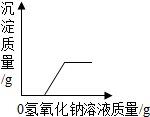 向一定质量的氯化铜和 稀盐酸的混合溶液中逐 渐加入氢氧化钠溶液 |
9.下列有关概念的辨析中正确的是( )
| A. | 分子是保持所有物质化学性质的最小微粒 | |
| B. | 催化剂一定能加快化学反应的速率 | |
| C. | 元素的种类是由原子的中子数决定的 | |
| D. | 由一种元素组成的物质可能是混合物 |
6.某实验小组利用废硫酸液制备K2SO4,设计的流程如图所示:
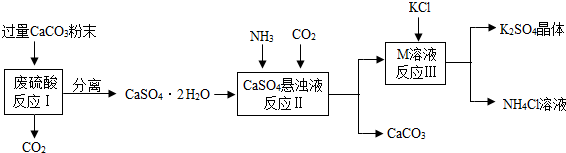
(1)写出1中加入CaCO3的原因与废硫酸液反应生成硫酸钙
(2)图中反应Ⅱ,Ⅲ后的操作名称是过滤;其中玻璃棒的作用是引流;
(3)反应Ⅲ中相关物质的溶解度如表所示:
则反应Ⅲ的化学方程式为:(NH4)2SO4+2KCl=2NH4Cl+K2SO4↓,该反应在常温下能发生的原因是:硫酸钾的溶解度最小;
(4)写出K2SO4在农业上的一点用途作钾肥.

(1)写出1中加入CaCO3的原因与废硫酸液反应生成硫酸钙
(2)图中反应Ⅱ,Ⅲ后的操作名称是过滤;其中玻璃棒的作用是引流;
(3)反应Ⅲ中相关物质的溶解度如表所示:
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)写出K2SO4在农业上的一点用途作钾肥.
7.分析处理图表信息是学习化学的一种重要方法.下表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
(1)40℃时,氯化钠的溶解度为36.6g.
(2)碳酸钠的溶解度随温度的升高而增大(填“增大”或“减小”).在20℃时,将100g的水加入30g碳酸钠中,充分搅拌后得到的是饱和溶液(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30℃,该溶液的溶质质量分数为23.1%(计算结果精确到0.1%).
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
(2)碳酸钠的溶解度随温度的升高而增大(填“增大”或“减小”).在20℃时,将100g的水加入30g碳酸钠中,充分搅拌后得到的是饱和溶液(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30℃,该溶液的溶质质量分数为23.1%(计算结果精确到0.1%).