题目内容
14.在托盘天平的两盘上各放一只烧杯,分别盛有等质量足量的稀盐酸,天平平衡.向左边烧杯中加入n克铁粉,向右边烧杯中加入n克镁和氧化镁的混合物,充分反应后,若天平仍然平衡,则混合物中镁和氧化镁的质量比为3:4.分析 根据天平仍然平衡,说明反应后生成的氢气一样多,据此可以计算出混合物中镁的质量和氧化镁的质量进行解答.
解答 解:设ng 铁粉产生氢气的质量为x.
Fe+2HCl=FeCl2+H2↑
56 2
ng x
$\frac{56}{ng}=\frac{2}{x}$
x=$\frac{n}{28}$g
设混合物中镁的质量为y
Mg+2HCl=MgCl2+H2↑
24 2
y $\frac{n}{28}$g
$\frac{24}{y}=\frac{2}{\frac{n}{28}g}$
y=$\frac{3}{7}n$g
所以混合物中氧化镁的质量为:ng-$\frac{3}{7}n$g=$\frac{4}{7}n$g
故混合物中镁与氧化镁的质量比是$\frac{3}{7}n$g:$\frac{4}{7}n$g=3:4.
故答案为:.
点评 本题主要考查有关化学方程式的计算和化学式的计算,难度较大.

练习册系列答案
相关题目
17.各种洗涤剂广泛进入人们的生活中,下列所用的洗涤剂不具有乳化作用的是( )
| A. | 用沐浴露洗澡 | B. | 用洗衣粉洗衣服 | ||
| C. | 用洗洁精洗餐具上的油污 | D. | 用汽油洗去手上的油污 |
5.完成下表(按氧化物、酸、碱、盐分类填写)
| 物质名称(或俗称) | 熟石灰 | 纯碱 | 硫酸 | ||
| 化学式 | CuSO4•5H2O | CaO | |||
| 分类 |
2.化学概念在逻辑上有如图所示关系时,对下列概念间的关系说法正确的是( )
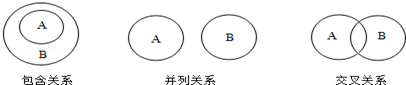
①纯净物与混合物属于包含关系
②化合物与氧化物属于包含关系
③单质与化合物属于交叉关系
④酸、碱、盐属于并列关系
⑤中和反应与复分解反应属于并列关系.

①纯净物与混合物属于包含关系
②化合物与氧化物属于包含关系
③单质与化合物属于交叉关系
④酸、碱、盐属于并列关系
⑤中和反应与复分解反应属于并列关系.
| A. | ①② | B. | ③④ | C. | ①⑤ | D. | ②④ |
9.铌酸锂(LiNbO3)是目前用途最广泛的新型无机材料之一.下列关于它的说法不正确的是( )
| A. | 铌酸锂是一种盐 | |
| B. | 铌酸锂是由五个原子构成的 | |
| C. | 铌酸锂是由铌、锂、氧三种元素组成的 | |
| D. | 铌酸锂中铌、锂、氧元素的质量比为93:7:48 |
3.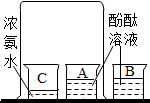 在课堂上,老师和同学们共同完成了如图所示实验,容器A中溶液变红,B中溶液不变色,该实验现象说明( )
在课堂上,老师和同学们共同完成了如图所示实验,容器A中溶液变红,B中溶液不变色,该实验现象说明( )
 在课堂上,老师和同学们共同完成了如图所示实验,容器A中溶液变红,B中溶液不变色,该实验现象说明( )
在课堂上,老师和同学们共同完成了如图所示实验,容器A中溶液变红,B中溶液不变色,该实验现象说明( )| A. | 分子可以分成原子,原子不能再分 | |
| B. | 分子在不断地运动,温度越高运动越快 | |
| C. | 氨气溶于水后溶液呈碱性 | |
| D. | 分子是化学变化中的最小微粒 |
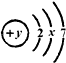 ,x=8,其中y=7;如果用A表示该元素,则它与+2价的B元素组成的化合物的化学式为:BA2.
,x=8,其中y=7;如果用A表示该元素,则它与+2价的B元素组成的化合物的化学式为:BA2. 如图所示,该装置在化学实验中有洗气、检验、收集、储气等多种用途:
如图所示,该装置在化学实验中有洗气、检验、收集、储气等多种用途: