题目内容
8.将下列符号中“2”所表示的意义写在横线上:(1)2Hg汞原子的个数为2 (2)SO42-一个硫酸根离子带有两个单位的负电荷(3)N21个氮分子中含有2个氮原子(4)$\stackrel{+2}{Cu}$O氧化铜中铜元素的化合价为+2价.
分析 (1)标在元素符号前面的数字表示原子的个数.
(2)标在元素符号右上角的数字表示1个离子所带的电荷数.
(3)标在化学式中元素右下角的数字表示一个分子中所含原子的数目.
(4)标在元素符号正上方的数字表示该元素化合价的数值.
解答 解:(1)标在元素符号前面的数字表示原子的个数,2Hg中的“2”表示汞原子的个数为2.
(2)标在元素符号右上角的数字表示1个离子所带的电荷数,SO42-中的“2”表示一个硫酸根离子带有两个单位的负电荷.
(3)标在化学式中元素右下角的数字表示一个分子中所含原子的数目,N2中的“2”表示1个氮分子中含有2个氮原子.
(4)标在元素符号正上方的数字表示该元素化合价的数值,$\stackrel{+2}{Cu}$O中的“2”表示氧化铜中铜元素的化合价为+2价.
故答案为:(1)汞原子的个数为2;(2)一个硫酸根离子带有两个单位的负电荷;(3)1个氮分子中含有2个氮原子;(4)氧化铜中铜元素的化合价为+2价.
点评 本题难度不大,主要考查了元素符号不同位置的数字表示的意义,掌握标在元素符号不同位置的数字所表示的意义是正确解答此类题的关键所在.

练习册系列答案
相关题目
16.现有一组物质:海水、生理盐水、碘酒,下列物质中,可以和这组物质归为不同类的是( )
| A. | 冰水混合物 | B. | 泥水 | C. | 雪碧 | D. | 肥皂水 |
18.某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
(1)测定过程中发生反应的化学方程式为Mg+H2SO4=MgSO4+H2↑.
(2)从以上数据可知,最后剩余的0.6g固体的成分是铜.这六次实验中,第5次加入稀硫酸时样品中的镁已经完全反应;表格中,m=2.5g.
(3)计算硫酸溶液的质量分数.
| 稀硫酸用量 | 剩余固体质量 | 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg | 第四次加入10g | 1.0g |
| 第二次加入10g | 2.0g | 第五次加入10g | 0.6g |
| 第三次加入10g | 1.5g | 第六次加入10g | 0.6g |
(2)从以上数据可知,最后剩余的0.6g固体的成分是铜.这六次实验中,第5次加入稀硫酸时样品中的镁已经完全反应;表格中,m=2.5g.
(3)计算硫酸溶液的质量分数.
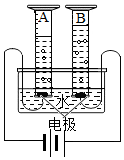 如图是一个电解水的装置,其中A中产生的是氢气气体,电解水实验的文字表达式是水$\stackrel{通电}{→}$氢气+氧气.
如图是一个电解水的装置,其中A中产生的是氢气气体,电解水实验的文字表达式是水$\stackrel{通电}{→}$氢气+氧气.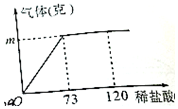 10克碳酸钙与稀盐酸反应,加入稀盐酸的质量与生成气体的质量关系如图所示
10克碳酸钙与稀盐酸反应,加入稀盐酸的质量与生成气体的质量关系如图所示