题目内容
19.为测定某硫酸溶液的溶质质量分数,化学小组的同学取硫酸溶液10g,向其中滴加过量的氯化钡溶液,过滤,得到沉淀4.66g.请计算:该硫酸溶液中溶质的质量分数.(温馨提示:H2SO4+BaCl2═BaSO4↓+2HCl)
分析 题目给出了生成的沉淀的质量为4.66g,根据硫酸钡的质量和对应的化学方程式求算硫酸中溶质的质量,进而求算其质量分数.
解答 解:设硫酸溶液中溶质的质量为x
H2SO4+BaCl2=BaSO4↓+2HCl
98 233
x 4.66g
$\frac{98}{233}$=$\frac{x}{4.66g}$
x=1.96g
硫酸溶液中溶质的质量分数为:$\frac{1.96g}{10g}×100%=19.6%$
答:硫酸溶液中溶质的质量分数为19.6%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
10.下列气体既可用浓硫酸干燥,又可用氢氧化钠固体干燥的是( )
| A. | CO | B. | HCl | C. | CO2 | D. | NH3 |
7.食品安全无小事,下列说法正确的是( )
| A. | 食用经高温处理后的霉变食物 | B. | 用亚硝酸钠代替食盐烹调 | ||
| C. | 用甲醛溶液浸泡海产品保鲜 | D. | 食用加铁酱油可强化营养 |
4.康康同学爱做家务劳动,他所做的家务劳动中包含化学变化的是( )
| A. | 用洗洁精刷碗 | B. | 用活性炭吸为冰箱除异味 | ||
| C. | 用小苏打蒸馒头 | D. | 把洗干净的衣服在阳光下晒干 |
8.对于下列化学用语,说法不正确的是( )
①H ②Mg ③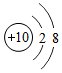 ④
④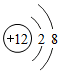 ⑤NaCl ⑥P2O5 ⑦CO32-.
⑤NaCl ⑥P2O5 ⑦CO32-.
①H ②Mg ③
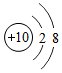 ④
④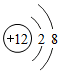 ⑤NaCl ⑥P2O5 ⑦CO32-.
⑤NaCl ⑥P2O5 ⑦CO32-.| A. | ①、②、③都可以表示原子 | |
| B. | ⑤和⑥既能表示物质的元素组成,又能表示该物质的一个分子 | |
| C. | ③和④所代表的微粒的化学性质相似 | |
| D. | 能表示离子的只有④和⑦ |
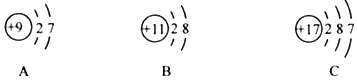
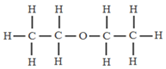 屠呦呦曾从西晋医学家葛洪的《肘后备急方》中获得灵感,她因此认识到不能用加热法提取青蒿素;于是改用低沸点的乙醚提取,终于在经历第190次失败后获得成功,并荣获2015年诺贝尔生理学或医学奖.请回答:
屠呦呦曾从西晋医学家葛洪的《肘后备急方》中获得灵感,她因此认识到不能用加热法提取青蒿素;于是改用低沸点的乙醚提取,终于在经历第190次失败后获得成功,并荣获2015年诺贝尔生理学或医学奖.请回答: