题目内容
 <1>经过一年化学知识的学习,我们可以初步认识到:化学反应的快慢、现象、生成物等与反应物的量有着密切关系.请各举一例说明:
<1>经过一年化学知识的学习,我们可以初步认识到:化学反应的快慢、现象、生成物等与反应物的量有着密切关系.请各举一例说明:(1)反应物的量不同,生成物可能不同
(2)反应物的量不同,反应现象可能不同
(3)反应温度不同,反应速率可能不同
<2>水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约水.
(1)“清洁用水,健康世界”,地下水(含一定量的Ca(HCO3)2,MgSO4和少量的FeCl3)会影响人的健康.我国规定生活饮用水的水质必须达到下述四项指标:
a.不得呈现异色 b.不得有异味 c.应澄清透明 d.不得含有细菌和病毒.其中“b指标”可以通过
(2)生活中可以采用
(3)新买的铝壶用来烧水时,内壁被水淹没处有黑色物质生成,底部则有白色物质生成.
①黑色物质是铁,其形成过程的化学方程式为
②白色物质是水垢[主要成分是CaCO3和Mg(OH)2],可用盐酸来除去,其中除去Mg(OH)2的反应方程式为
(4)水的用途广泛,许多化学实验中用到水,请你列举一例:
(5)下列各种水中属于纯净物的是
①矿泉水 ②自来水 ③蒸馏水 ④汽水 ⑤糖水
(6)小明家长期饮用“××牌纯净水”,专家认为这是不科学的,理由是
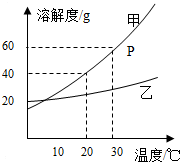
<3>如图是甲乙两种固体物质的溶解度曲线.据图回答:(1)P点的含义是:
(2)20℃时要使接近饱和的甲溶液变成饱和溶液,可以采用的方法有
(3)当甲中含有少量乙时,可采用
(4)30℃时,将40g甲物质放入盛有50g水的烧杯中,所得溶液溶质的质量分数为
A.溶剂的质量 B.溶液的质量 C.溶质的质量分数 D.以上都不变.
考点:实验探究物质变化的条件和影响物质变化的因素,结晶的原理、方法及其应用,水的性质和应用,水的净化,硬水与软水,饱和溶液和不饱和溶液相互转变的方法,固体溶解度曲线及其作用,金属的化学性质
专题:溶液、浊液与溶解度,空气与水,科学探究
分析:根据已有的化学反应分析解答即可;根据净水中过程中各物质的作用和操作进行分解答;根据溶解度曲线的意义以及溶液的知识分析解答即可.
解答:解;<1>(1)氧气充足时碳燃烧生成二氧化碳,氧气不充足时碳燃烧生成一氧化碳,故填:碳在氧气中充分燃烧和不充分燃烧;
(2)硫在空气中燃烧发出淡蓝色的火焰,在氧气中燃烧发出蓝紫色的火焰,故填:硫在空气和氧气中燃烧;
(3)过氧化氢溶液在常温下分解的速度很慢,加热能加快过氧化氢的分解,故填:过氧化氢溶液在常温和加热的条件下分解速率不同;
<2>(1)除去异味可以利用活性炭的吸附作用,故填:吸附;
(2)鉴别硬水和软水使用的是肥皂水,加热煮沸能将水中可溶性钙镁化合物转化为不溶性钙镁化合物,从而降低水的硬度,故填:肥皂水,煮沸;
(3)①铝能与氯化铁反应生成氯化铝和铁,故填:FeCl3+Al=AlCl3+Fe;
②盐酸能与氢氧化镁反应生成氯化镁和水,该反应属于复分解反应,故填:2HCl+Mg(OH)2═MgCl2+2H2O,复分解反应;
(4)在实验室中水常用于配制溶液,故填:配制溶液;
(5)①矿泉水属于混合物,②自来水属于混合物,③蒸馏水属于纯净物,④汽水属于混合物,⑤糖水属于混合物,故填:③;
(6)长期饮用纯净水不利于人体健康,因为纯净水中含有的人体所需要的矿物质太少,故填:因为纯净水中矿物质含量太少,长期饮用不利于人体健康.
<3>(1)据图可以看出,P点表示的是30℃时,甲的溶解度为60g,故填:30℃时,甲的溶解度为60g;
(2)20℃时要使接近饱和的甲溶液变成饱和溶液,可以采取降低温度的方法,故填:降低温度;
(3)甲的溶解度受温度影响变化大,故当甲中含有少量乙时,可采用降低结晶的方法提纯甲,故填:降温结晶;
(4)30℃时,将40g甲物质放入盛有50g水的烧杯中,只能溶解30g甲,故其溶质质量分数为:
×100%=37.5%;若将烧杯内物质升温到50℃,则溶质溶解,溶液质量增加,溶质质量分数变大,故填:B、C.
(2)硫在空气中燃烧发出淡蓝色的火焰,在氧气中燃烧发出蓝紫色的火焰,故填:硫在空气和氧气中燃烧;
(3)过氧化氢溶液在常温下分解的速度很慢,加热能加快过氧化氢的分解,故填:过氧化氢溶液在常温和加热的条件下分解速率不同;
<2>(1)除去异味可以利用活性炭的吸附作用,故填:吸附;
(2)鉴别硬水和软水使用的是肥皂水,加热煮沸能将水中可溶性钙镁化合物转化为不溶性钙镁化合物,从而降低水的硬度,故填:肥皂水,煮沸;
(3)①铝能与氯化铁反应生成氯化铝和铁,故填:FeCl3+Al=AlCl3+Fe;
②盐酸能与氢氧化镁反应生成氯化镁和水,该反应属于复分解反应,故填:2HCl+Mg(OH)2═MgCl2+2H2O,复分解反应;
(4)在实验室中水常用于配制溶液,故填:配制溶液;
(5)①矿泉水属于混合物,②自来水属于混合物,③蒸馏水属于纯净物,④汽水属于混合物,⑤糖水属于混合物,故填:③;
(6)长期饮用纯净水不利于人体健康,因为纯净水中含有的人体所需要的矿物质太少,故填:因为纯净水中矿物质含量太少,长期饮用不利于人体健康.
<3>(1)据图可以看出,P点表示的是30℃时,甲的溶解度为60g,故填:30℃时,甲的溶解度为60g;
(2)20℃时要使接近饱和的甲溶液变成饱和溶液,可以采取降低温度的方法,故填:降低温度;
(3)甲的溶解度受温度影响变化大,故当甲中含有少量乙时,可采用降低结晶的方法提纯甲,故填:降温结晶;
(4)30℃时,将40g甲物质放入盛有50g水的烧杯中,只能溶解30g甲,故其溶质质量分数为:
| 30g |
| 30g+50g |
点评:本题考查的是影响化学反应现象、生成物的因素、水的净化以及溶解度的知识,解答本题可以依据已有的知识结合题干提供的信息进行.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
下列括号中对日常生活的变化判断正确的是( )
| A、玻璃窗破裂(化学变化) |
| B、蜡烛燃烧(化学变化) |
| C、二氧化碳使澄清的石灰水变浑浊(物理变化) |
| D、蜡烛融化(化学变化) |
学习化学以后,大家学会了从化学的视角观察生活和分析问题.以下说法正确的是( )
| A、绿色食品不含任何化学物质 |
| B、“过滤”能将硬水转化成软水 |
| C、用干冰作食品的制冷剂 |
| D、加碘食盐中的“碘”应理解为碘原子 |
不能把N2和CO2鉴别开的操作是( )
| A、通入澄清的石灰水 |
| B、通入高温下的木炭 |
| C、伸入燃着的木条 |
| D、降低温度,使之变成固体 |
科学家最近研制出利用太阳能产生激光,并在催化剂作用下使海水分解得到氢气的新技术.下列说法不正确的是( )
A、该技术使水分解的化学方程式为:2H2O
| ||||
| B、水分解产生氢气的同时释放出巨大的能量 | ||||
| C、该技术可以将太阳能转化为氢能源 | ||||
| D、水分解和氢气燃烧都不会产生污染 |
 ,镁原子在化学反应中容易
,镁原子在化学反应中容易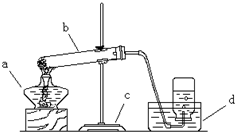 某校研究性学习小组到实验室进行探究实验.他们准备用加热高锰酸钾的方法制取氧气并验证氧气的性质.
某校研究性学习小组到实验室进行探究实验.他们准备用加热高锰酸钾的方法制取氧气并验证氧气的性质.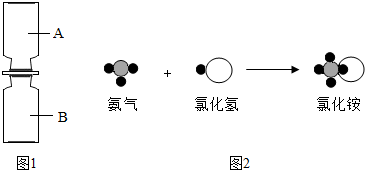
 ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用图2表示,该反应的化学方程式为
”表示氯原子,上述反应过程可用图2表示,该反应的化学方程式为