题目内容
11.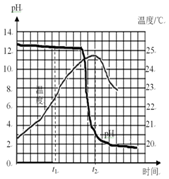 为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:
为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:(1)由pH变化图象可知,在t1时刻,烧杯中存在的阴离子是Cl-和OH-(写离子符号).
(2)由温度变化图象可知,稀盐酸和氢氧化钠溶液发生的化学反应是放热(选填“放热”或“吸热”)反应.t2时刻后,溶液温度降低的主要原因是反应结束了.
(3)上述实验产物为氯化钠,实验小组还想测量一定质量大颗粒食盐晶体的体积.在量筒内倒入一定量的水,然后将一定质量的食盐晶体放入,观察液面的变化来测量食盐的体积,但他的想法马上遭到大家的否定,原因是食盐易溶于水.最后同学换成另一种液体
才取得实验成功.
分析 (1)根据此时溶液的酸碱度及反应中的物质解答;
(2)根据温度变化图象可知,稀盐酸和氢氧化钠溶液发生放出热量;
(3)根据食盐易溶于水进行分析.
解答 解:(1)由pH变化图象可知,在t1时刻,溶液显碱性,溶液中阴离子有氢氧根离子和氯离子;
(2)由温度变化图象可知,稀盐酸和氢氧化钠溶液发生的反应放出热量;t2时刻后,溶液温度降低的主要原因是反应结束了.
(3)因为食盐易溶于水,所以不能将一定质量的食盐晶体放入盛有一定量的水的量筒内,来测量食盐的体积;
故答案为:(1)Cl-和OH-(2)放热;反应结束了;(3)食盐易溶于水.
点评 本题考查了化学知识在医药方面的应用,完成此题,可以依据酸和碱反应的有关知识进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.编制第一个元素周期表的科学家是( )
| A. | 道尔顿 | B. | 卢瑟福 | C. | 门捷列夫 | D. | 汤姆森 |
19.通过对已学知识的对比和归纳,可以得出一些十分有趣的规律.这些规律可以帮助我们掌握学习化学的方法.请你仔细阅读表中的内容,并回答相应的问题.
(1)由表格内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的电荷数相等;
(2)硫酸亚铁受热能分解,产物均为氧化物,唯一的固体产物呈红色,结合表中信息和反应原理,写出该分解反应产物的化学式:Fe2O3、SO2、SO3;.
| 常见元素或原子团 | OH- | SO42- | CO32- | H元素 | Na元素 | Cl元素 | Fe元素 | S元素 |
| 常见化合价 | -1 | -2 | -2 | +1 | +1 | -1、+5、+7 | +2、+3 | -2、+4、+6 |
(2)硫酸亚铁受热能分解,产物均为氧化物,唯一的固体产物呈红色,结合表中信息和反应原理,写出该分解反应产物的化学式:Fe2O3、SO2、SO3;.
6.下列对有关溶液知识的解释不正确的是( )
| A. | 饱和溶液析出晶体后,溶质的质量分数可能不变 | |
| B. | “冬天捞碱,夏天晒盐”的主要原理是不同物质的溶解度随温度变化不同 | |
| C. | 不饱和溶液转化为饱和溶液,其溶质质量分数一定变大 | |
| D. | 向氯化铁溶液中加入少量生石灰,原溶液中溶质的溶解度和溶质质量分数都发生变化 |
16.下列说法正确的是( )
| A. | 氢氧化镁中有氢氧根离子,加入酚酞会显红色 | |
| B. | 甲烷是热气球的一种常用燃料,说明其具有助燃性 | |
| C. | 冰水混合物属于纯净物,从微观上看是因为只含有一种分子 | |
| D. | 5ml酒精和5ml水混合体积小于10ml,是因为分子中有空隙 |
1.逻辑推理是化学学习常用的思维方法.下列推理正确的是( )
| A. | 酸溶液的pH都小于7,所以pH小于7 的一定是酸溶液 | |
| B. | 单质中只含一种元素,所以含一种元素的物质一定是单质 | |
| C. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 | |
| D. | 中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应 |
