题目内容
16.如图为某分子的结构模型,请回答下列问题: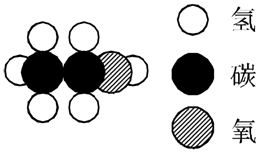
(1)这种分子的化学式为C2H6O;该物质是白酒的主要成分,化学名称为酒精(或乙醇).
(2)该物质中碳、氢、氧原子个数比为2:6:1.
(3)该物质中氧元素的质量分数为34.8%.(结果保留到0.1%)
分析 (1)根据分子结构模型来分析其化学式;
(2)根据该物质的分子结构来分析;
(3)根据化合物中,元素质量分数的计算方法来分析.
解答 解:(1)由分子结构模型可知,该物质的1个分子是由2个碳原子、6个氢原子和1个氧原子构成的,其化学式为C2H6O,白酒是酒精(或乙醇)的水溶液;故填:C2H6O;酒精(或乙醇);
(2)由乙醇的化学式可知,1个乙醇分子是由2个碳原子、6个氢原子和1个氧原子构成的,故填:2:6:1;
(3)由乙醇的化学式可知,其中氧元素的质量分数为:$\frac{16}{12×2+1×6+16}×100%$≈34.8%.故填:34.8%.
点评 本题主要考查了物质的微观构成方面的问题,充分利用微观示意图中所表现出来的信息是解题的关键.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
6.2016年,南京大学邹志刚课题组及其合作者利用ZnGa2O4介孔光催化材料用于CO2的光还原,成功实现了将CO2转化为碳氢化合物燃料.该反应化学方程式为CO2+2H2O$\frac{ZnGa_{2}O_{4}}{\;}$CH4+2O2.下列有关该反应说法错误的是( )
| A. | 此反应属于置换反应 | |
| B. | 此反应前后分子个数不变 | |
| C. | 此反应为CO2的利用创造一种新的方法 | |
| D. | 此反应制取的CH4可以再生利用 |
7.下列说法中正确的是( )
| A. | 碳酸盐与酸反应生成气体,与酸反应生成气体的物质一定是碳酸盐 | |
| B. | CO2能使燃着的木条熄灭,所以能使燃着的木条熄灭一定是CO2 | |
| C. | 中和反应生成盐和水,所以生成盐和水生成的反应一定是中和反应 | |
| D. | 酸性溶液是紫色石蕊溶液变红色,所以使紫色石蕊溶液变红的溶液一定是酸性溶液 |
4.下列有关生活、生产中的一些做法,其中合理的是( )
| A. | 用熟石灰改良酸性土壤 | |
| B. | 把NH4NO3和草木灰(主要成分K2CO3,呈碱性)混合施用增加肥效 | |
| C. | 及时除去铝制品表面氧化膜防止进一步锈蚀 | |
| D. | 误食含重金属离子食物后马上饮用大量水解毒 |
1.选用括号内的试剂或方法鉴别下列各组物质,其中不正确的是( )
| A. | 羊毛和涤纶(灼烧,闻气味) | B. | 淀粉和葡萄糖(加碘水) | ||
| C. | 硫酸铵和氯化铵(加熟石灰粉末研磨) | D. | 氧化钙和氢氧化钙(加水) |
8.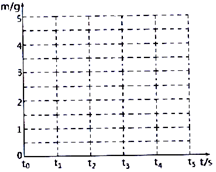 某化学兴趣小组的同学把12g石灰石样品和100g稀盐酸(足量)放入烧杯中,在化学反应过程中对烧杯及其中剩余物进行六次称量,记录数据如表(杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25g)
某化学兴趣小组的同学把12g石灰石样品和100g稀盐酸(足量)放入烧杯中,在化学反应过程中对烧杯及其中剩余物进行六次称量,记录数据如表(杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25g)
(1)反应共生成了二氧化碳4.4g,请计算石灰石样品中碳酸钙的质量是多少?
(2)反应完全后所得溶液中氯化钙的溶质质量分数(计算结果精确至0.1%)
(3)请在如图坐标图中画出生成的气体质量(m)随时间(t)变化的曲线.
 某化学兴趣小组的同学把12g石灰石样品和100g稀盐酸(足量)放入烧杯中,在化学反应过程中对烧杯及其中剩余物进行六次称量,记录数据如表(杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25g)
某化学兴趣小组的同学把12g石灰石样品和100g稀盐酸(足量)放入烧杯中,在化学反应过程中对烧杯及其中剩余物进行六次称量,记录数据如表(杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25g)| 反应时间(s) | t0 | t1 | t2 | t3 | t4 | t5 |
| 烧杯和药品质量(g) | 137 | 135 | 133.5 | 133 | 132.6 | 132.6 |
(2)反应完全后所得溶液中氯化钙的溶质质量分数(计算结果精确至0.1%)
(3)请在如图坐标图中画出生成的气体质量(m)随时间(t)变化的曲线.
5.下列实验方案,设计合理的是( )
| A. | 除去KNO3溶液中混有的少量K2SO4:选用BaCl2溶液 | |
| B. | 制备Cu(OH)2:将CuSO4溶液和Ba(OH)2溶液混合后过滤 | |
| C. | 验证质量守恒定律:将镁条在氧气中燃烧,比较反应前后固体的质量 | |
| D. | 鉴别NaOH溶液和Ca(OH)2溶液:取样后,分别通入二氧化碳气体 |
6.下列方法能鉴别空气、氧气和二氧化碳3 瓶气体的是( )
| A. | 用带火星的小木条 | B. | 澄清石灰水 | ||
| C. | 看颜色 | D. | 将燃着的木条伸入集气瓶中 |
 如图是两种化肥标签的一部分,请回答:
如图是两种化肥标签的一部分,请回答: