题目内容
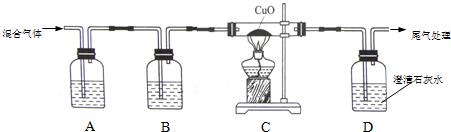
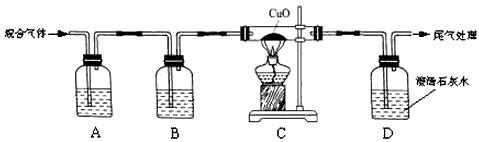
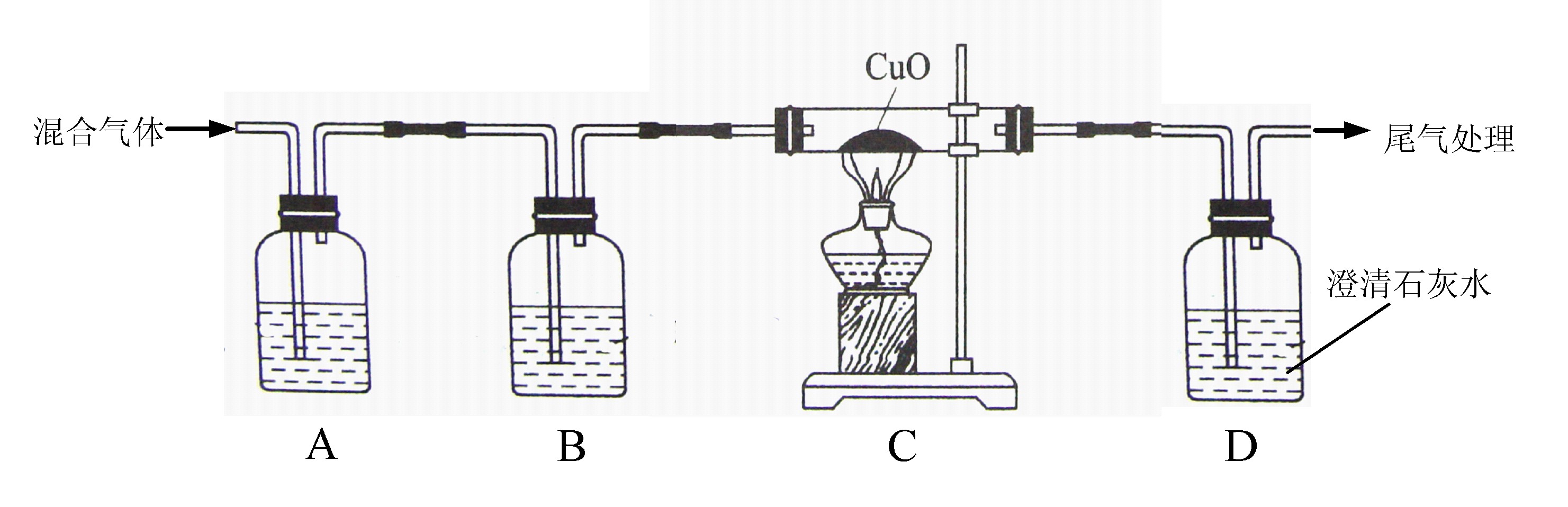
下图所示装置可以验证某混合气体(无色无味)是否含有CO2和CO.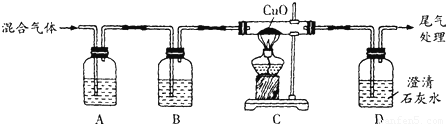
请回答下列问题:
(1)A装置中的试剂是 (写名称,下同),B装置中的试剂是 .
(2)证明原混合气体中CO2存在的实验现象是 .证明原混合气体中CO存在的实验现象是 .
(3)如果没有B装置,对实验结果有何影响? .
(4)请设计实验证明原B瓶中的液体与CO2已经发生了化学反应.
| 实验操作 | 实验现象 | 写出有关化学方程式 |
【答案】分析:(1)使澄清石灰水变浑浊是CO2的特性,所以装置A中的试剂为澄清石灰水;验证CO往往是验证其与氧化铜反应后有无CO2生成,但在与氧化铜反应之前,应把混合气体中的CO2完全除净,否则将无法证明反应后所含有的CO2是反应生成的,还是反应前就有的,所以装置B中盛放的应能吸收CO2的NaOH溶液;
(2)据二氧化碳和一氧化碳的性质分析解答;
(3)如果没有B装置,就不能除去二氧化碳,无法证明使D瓶澄清的石灰水变浑浊二氧化碳是一氧化碳与氧化铜反应产生的,从而不能证明有一氧化碳存在;
(4)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,可据碳酸钠遇酸生成二氧化碳,或与可溶性的钙盐反应生成碳酸钙沉淀设计实验.
解答:解:(1)使澄清石灰水变浑浊是CO2的特性,装置A是用来检验二氧化碳的,故A中的试剂为澄清石灰水;B装置是用来吸收二氧化碳的,故应为氢氧化钠溶液;
(2)证明原混合气体中CO2存在的实验现象是A中澄清石灰水变浑浊;证明原混合气体中CO存在的实验现象是C中黑色粉末变红,D中澄清石灰水变浑浊,注意两种现象缺一不可;
(3)验证CO往往是验证其与氧化铜反应后有无CO2生成,但在与氧化铜反应之前,应把混合气体中的CO2完全除净,否则将无法证明反应后所含有的CO2是反应生成的,还是反应前就有的,故没有B装置,无法除掉CO2,从而无法判断原混合气体中是否含有CO气体;
(4)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,要证明二氧化碳与氢氧化钠溶液反应,就是证明碳酸钠的存在,可向反应后的溶液中加入CaCl2溶液,若有白色沉淀生成,证明二者反应,方程式是:CaCl2+Na2CO3═2NaCl+CaCO3↓;
故答案为:(1)澄清石灰水,氢氧化钠溶液;
(2)A瓶中澄清的石灰水变浑浊; C装置中黑色粉末变成红色,D瓶澄清的石灰水变浑浊;
(3)不能证明使D瓶澄清的石灰水变浑浊二氧化碳是一氧化碳与氧化铜反应产生的,从而不能证明有一氧化碳存在;
(4)实验操作:向反应后的液体中加入CaCl2溶液;
实验现象:有白色沉淀生成;
方程式:CaCl2+Na2CO3═2NaCl+CaCO3↓.(合理均可)
点评:此题主要考查同学们的综合分析能力,不但要求同学们具备有关物质的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时要认真分析题目给出的条件,联系实际,逐一分析推断.
(2)据二氧化碳和一氧化碳的性质分析解答;
(3)如果没有B装置,就不能除去二氧化碳,无法证明使D瓶澄清的石灰水变浑浊二氧化碳是一氧化碳与氧化铜反应产生的,从而不能证明有一氧化碳存在;
(4)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,可据碳酸钠遇酸生成二氧化碳,或与可溶性的钙盐反应生成碳酸钙沉淀设计实验.
解答:解:(1)使澄清石灰水变浑浊是CO2的特性,装置A是用来检验二氧化碳的,故A中的试剂为澄清石灰水;B装置是用来吸收二氧化碳的,故应为氢氧化钠溶液;
(2)证明原混合气体中CO2存在的实验现象是A中澄清石灰水变浑浊;证明原混合气体中CO存在的实验现象是C中黑色粉末变红,D中澄清石灰水变浑浊,注意两种现象缺一不可;
(3)验证CO往往是验证其与氧化铜反应后有无CO2生成,但在与氧化铜反应之前,应把混合气体中的CO2完全除净,否则将无法证明反应后所含有的CO2是反应生成的,还是反应前就有的,故没有B装置,无法除掉CO2,从而无法判断原混合气体中是否含有CO气体;
(4)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,要证明二氧化碳与氢氧化钠溶液反应,就是证明碳酸钠的存在,可向反应后的溶液中加入CaCl2溶液,若有白色沉淀生成,证明二者反应,方程式是:CaCl2+Na2CO3═2NaCl+CaCO3↓;
故答案为:(1)澄清石灰水,氢氧化钠溶液;
(2)A瓶中澄清的石灰水变浑浊; C装置中黑色粉末变成红色,D瓶澄清的石灰水变浑浊;
(3)不能证明使D瓶澄清的石灰水变浑浊二氧化碳是一氧化碳与氧化铜反应产生的,从而不能证明有一氧化碳存在;
(4)实验操作:向反应后的液体中加入CaCl2溶液;
实验现象:有白色沉淀生成;
方程式:CaCl2+Na2CO3═2NaCl+CaCO3↓.(合理均可)
点评:此题主要考查同学们的综合分析能力,不但要求同学们具备有关物质的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目