题目内容
10.能证明分子在化学反应中可分的是( )| A. | 加热氧化汞有汞和氧气生成 | B. | 碘加热升华成气体 | ||
| C. | 蜡烛熔化 | D. | 加热水产生蒸汽 |
分析 能证明分子在化学反应中可分说明该变化必须是化学变化,有新物质生成的属于化学变化
解答 解:A、加热氧化汞有汞和氧气生成,有新物质生成,属于化学变化,故A正确;
B、碘受热升华由固态变为气态,只是状态发生了变化,没有新物质生成,属于物理变化,故B错误;
C、蜡烛熔化,是由固态变为液态,只是状态发生了变化,属于物理变化,故C错误;
D、加热水产生蒸汽,是由液态变为气态,只是状态发生了变化,没有新物质生成,属于物理变化,故D错误.
故选A.
点评 解答本题关键是要知道证明分子在化学反应中可分必须是通过化学变化来证明.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
18.下列有关实验操作的快慢先后,说法错误的是( )
| A. | 测量空气中氧气的含量时,点燃红磷后要迅速伸入集气瓶中 | |
| B. | 用排水法收集氧气时,先把导管放入装满水的集气瓶中,再开始加热 | |
| C. | 把点燃的木炭放入燃烧匙内,由上而下缓慢伸入集满氧气的集气瓶中 | |
| D. | 连接橡胶管和玻璃管时,应先用水润湿玻璃管一端,再慢慢的转入橡胶管中 |
5.下列元素名称与相应符号书写都正确的是( )
| A. | 炭 C | B. | 氮 N | C. | 钠 na | D. | 镁 Fe |
2.空气中氧气含量测定的再认识.
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.

(1)写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生镑的原理设计图2验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
【交流表达】
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据上表数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:
①铁的缓慢氧化使集气瓶中的氧气消耗更彻底,使实验结果更准确;
②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.

(1)写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生镑的原理设计图2验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据上表数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:
①铁的缓慢氧化使集气瓶中的氧气消耗更彻底,使实验结果更准确;
②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.
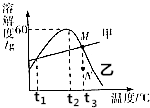 如图是甲、乙两种化合物的溶解度曲线示意图,据此得到的结论正确的是C.
如图是甲、乙两种化合物的溶解度曲线示意图,据此得到的结论正确的是C.

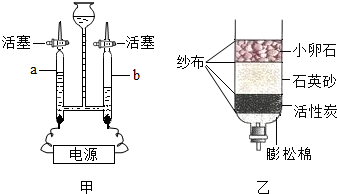 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.