题目内容
10. 组成相似的盐具有一些相似的化学性质.
组成相似的盐具有一些相似的化学性质.(1)①Cu(NO3)2溶液和CuSO4溶液都含有大量Cu2+(填离子符号).
②向Cu(NO3)2溶液中加入NaOH溶液,充分振荡.反应的化学方程式为Cu(NO3)2+2NaOH═Cu(OH)2↓+2NaNO3.
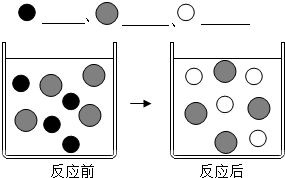
③向CuSO4溶液中加入过量的锌片,如图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子
 :Cu2+、
:Cu2+、 :SO42-、
:SO42-、 :Zn2+;(填离子符号)
:Zn2+;(填离子符号)(2)除上述实验外,在溶液中与Cu(NO3)2和CuSO4均能反应的物质还有Fe、KOH(任举二例不同类别的物质,填化学式,下同)
(3)在溶液中能与CuSO4反应而不与Cu(NO3)2反应的物质有Ba(NO3)2(任举一例).
分析 (1)①根据盐的组成写出含有的离子符号;
②根据碱和盐生成新碱和新盐写出反应的化学方程式;
③根据在金属活动性顺序中,锌排在铜之前,所以锌会和硫酸铜反应生成铜和硫酸锌;
(2)根据在金属活动性顺序中,排在铜之前的金属,可以将铜离子置换出来解答;
(3)根据硝酸钡和硫酸铜反应生成硝酸铜和硫酸钡白色沉淀,硝酸钡和硝酸铜不反应解答.
解答 解:(1)①Cu(NO3)2溶液和CuSO4溶液都含有大量Cu2+;
②Cu(NO3)2溶液中加入NaOH溶液,充分振荡.反应的化学方程式为Cu(NO3)2+2NaOH═Cu(OH)2↓+2NaNO3;
③根据在金属活动性顺序中,锌排在铜之前,所以锌会和硫酸铜反应生成铜和硫酸锌;锌片表面出现红色物质,溶液由蓝色变为无色,而锌片过量,所以溶液中没有硫酸铜剩余,只含有生成的硫酸锌,故每种图形代表的离子分别是: :Cu2+、
:Cu2+、 :SO42-、
:SO42-、 :Zn2+;
:Zn2+;
(2)根据在金属活动性顺序中,铁排在铜之前,可以将铜离子置换出来,氢氧化钾能够和铜离子反应生成沉淀;
(3)硝酸钡和硫酸铜反应生成硝酸铜和硫酸钡白色沉淀,硝酸钡和硝酸铜不反应.
答案:(1)①Cu2+;
②Cu(NO3)2+2NaOH═Cu(OH)2↓+2NaNO3;
③ :Cu2+、
:Cu2+、 :SO42-、
:SO42-、 :Zn2+;
:Zn2+;
(2)Fe;KOH;
(3)Ba(NO3)2.
点评 要想解答好这类题目,首先,要理解和熟记酸的化学性质、用途、反应现象和化学方程式,以及与之相关的知识.然后,根据所给的实验、问题情景结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
20.某同学设计的下列各实验方案中,你认为不能达到实验目的是( )
| A. | 除去硫酸镁溶液中混有的少量硫酸和硫酸铜,加入足量镁粉 | |
| B. | 除去CaCl2溶液中的HCl,加入过量的碳酸钙 | |
| C. | 鉴别涤纶和羊毛面料,分别取样灼烧、闻气味 | |
| D. | 除去氯化氢气体中的水蒸气,用氢氧化钠固体 |
1.下列离子能在pH=11的溶液中大量共存的是( )
| A. | K+、OH-、SO42-、Cu2+ | B. | CO32-、K+、Cl-、H+ | ||
| C. | H+、Ba2+、Cl-、SO42- | D. | K+、NO3-、Na+、OH- |
5.下列推论正确的是( )
| A. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 | |
| B. | 复分解反应的条件是:生成物有水、气体、沉淀三个条件至少满足一个,复分解反应才能发生 | |
| C. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| D. | 碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液呈碱性 |
15.下列各组物质按照单质、氧化物、混合物的顺序排列的是( )
| A. | 冰、干冰、天然气 | B. | 氮气、氧气、空气 | ||
| C. | 水银、水、碘酒 | D. | 石墨、熟石灰、盐酸 |
19.规范的操作是实验成功的保证,下列实验操作正确的是( )
| A. | 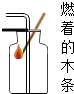 CO2验满 | B. | 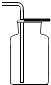 收集CO2 | C. | 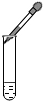 滴加液体 | D. | 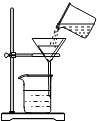 过滤 |
20.甲、乙、丙、丁表示四种物质,其微观示意图如表,甲和乙在一定条件下反应生成丙和丁.下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |  |
| 微观示意图 |  | 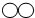 |  |  |
| A. | 甲、丁的化学式相同 | |
| B. | 只有丙物质属于单质 | |
| C. | 参加反应的甲与乙的分子个数比是2:1 | |
| D. | 反应中,反应物分子中所含氧原子总数是生成物分子中所含氧原子总数的2倍 |