题目内容
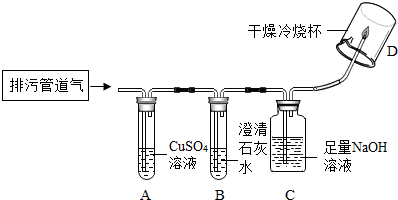
6. 工业用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙).简易流程如右图,主要的反应为:2CaCO3+2SO2+O2═2CaSO4+2X.
工业用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙).简易流程如右图,主要的反应为:2CaCO3+2SO2+O2═2CaSO4+2X.(1)流程中石灰石加水制成石灰浆的目的是便于吸收二氧化硫.反应中X的化学式为CO2,硫元素的化合价在反应前后的变化为由+4变为+6.
(2)减少二氧化硫的排放,主要为了B(填序号).
A.减缓温室效应 B.减少酸雨形成 C.防止破坏臭氧层
(3)按上述方法处理2000吨废气中的二氧化硫,至少需要含5吨碳酸钙的石灰石浆.求废气中二氧化硫的质量分数.
分析 (1)根据化学反应前后原子的种类与数目保持不变可以判断物质的化学式;
(2)二氧化硫可以形成酸雨解答;
(3)根据石灰石浆吸收废气中的二氧化硫的反应方程式找到碳酸钙与二氧化硫的比例关系,根据碳酸钙的质量即可求得所选二氧化硫的质量.
解答 解:(1)流程中石灰石加水制成石灰石浆的目的是便于吸收二氧化硫,根据2CaCO3+2SO2+O2═2CaSO4+2x可知,依据质量守恒定律可知每个x中含有1个碳原子和2个氧原子,所以x是二氧化碳.化学式是:CO2;
硫元素的化合价在反应前为+4,反应后为+6,反应前后的变化为由+4变为+6;
(2)A、温室效应主要是二氧化碳等温室气体排放到空气中形成的,与二氧化硫的排放无关,故选项错误.
B、煤等燃料燃烧生成二氧化硫、二氧化氮等溶于水是形成酸雨的主要原因,与二氧化硫的排放有关,故选项正确.
C、臭氧层破坏是含氟制冷剂排放到空气中造成的,与二氧化硫的排放无关,故选项错误.
(3)设废气中二氧化硫的质量为x.则
2CaCO3+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2,
200 128
5t x
$\frac{200}{128}=\frac{5t}{x}$解得:x=3.2t
废气中SO2的质量分数=$\frac{3.2t}{2000t}×100%$=0.16%
答案:(1)便于吸收二氧化硫;CO2,由+4变为+6;(2)B;(3)废气中SO2的质量分数为0.16%.
点评 解答本题要充分理解质量守恒定律和各种物质的性质等方面的内容,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
16.比较、分析、归纳是学习化学的重要方法.通过比较可以发现相同的反应物在不同外界条件下,会发生不同的反应.请参照示例归纳反应规律
| 组别 | 化学方程式 | 规律 |
| 示例 | C+O2(充足)$\frac{\underline{\;点燃\;}}{\;}$CO2 C+O2(不充足)$\frac{\underline{\;点燃\;}}{\;}$2CO2 | 反应物相同时,反应物的量不同,生成物不同. |
| (1) | 4Na+O2═2Na2O 4Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2 | |
| (2) | 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O Cu+4HNO3(浓)═3Cu(NO3)2+2NO2↑+2H2O |
17.俗话说:“人要实,火要虚”,烧木材时通常要把木材架空一些,木材燃烧得更旺,这是因为( )
| A. | 使木材与空气充分接触 | B. | 木材是可燃物 | ||
| C. | 温度易达到着火点 | D. | 散热快 |
4. 下列叙述不符合如图所示实验设计意图的是( )
下列叙述不符合如图所示实验设计意图的是( )
 下列叙述不符合如图所示实验设计意图的是( )
下列叙述不符合如图所示实验设计意图的是( )| A. | 说明一氧化碳具有还原性 | |
| B. | 说明生成物二氧化碳的密度比空气大 | |
| C. | 说明一氧化碳和氧化铜的反应需要加热 | |
| D. | 可以防止有毒的一氧化碳气体对空气的污染 |